Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
OSTEONECROSIS DEL MAXILAR EN PACIENTE CON MIELOMA MÚLTIPLE TRATADO CON BISFOSFONATOS
MŞ Victoria Cuevas Ruiz1, Ignacio Martínez Sancho2, Miriam Fernández Zubiaga3, María Zamora González-Marińo2, Olga Álamo González5
1Servicios de Hematología, 3Medicina Interna y 5Farmacia del Complejo Asistencial de Burgos
2Atención Primaria de Burgos. Espańa.
mvcuevas @ hgy.es
Rev Electron Biomed / Electron J Biomed 2006;3:14-28.
Comentario del revisor Prof. Francisco Abad Santos MD. PhD. Servicio de Farmacología Clínica. Hospital la Princesa. Departamento de Farmacología y Terapéutica de la Facultad de Medicina. Universidad Autónoma de Madrid. Espańa
Comentario del revisor María Jesús Coma del Corral MD. PhD. Responsable de la Unidad de Investigación del Hospital General Yagüe de Burgos. Espańa. Editora.
INTRODUCCIÓN:
Los bisfosfonatos son fármacos utilizados en el tratamiento y prevención de la osteoporosis posmenopáusica y la inducida por corticoides, en la enfermedad de Paget y en la hipercalcemia asociada a neoplasias; así mismo, están indicados en el tratamiento de las lesiones osteolíticas y del dolor provocado por las mismas.
En Hematología son usados en el tratamiento de los pacientes con mieloma que presentan lesiones osteolíticas y osteoporosis. Los bisfosfonatos más utilizados en estos pacientes son el pamidronato y el ácido zoledrónico. El pamidronato es administrado cada 3 o 4 semanas a la dosis de 90 mg durante un período de 2 horas o más, mientras que el ácido zoledrónico (con una mayor potencia), es administrado a la dosis de 4 mg durante 15 minutos, ambos vía endovenosa. El tiempo de infusión más corto para ácido zoledrónico ha supuesto una ventaja significativa sobre el pamidronato y, en la mayoría de los pacientes que recibían pamidronato éste se sustituyó por ácido zoledrónico en cuanto estuvo disponible.
Los bisfosfonatos son análogos sintéticos del pirofosfato inorgánico que tiene una alta afinidad por el calcio. Esta característica condiciona el depósito del fármaco en la matriz mineralizada ósea durante largos períodos de tiempo. Su mecanismo de acción se basa en que se fijan a la hidroxiapatita con lo que inhiben la resorción ósea osteoclástica, sin intervenir en la formación y mineralización del hueso; así mismo, frenan la liberación de calcio óseo inducido por factores estimulantes liberados por las células tumorales. Ciertos bisfosfonatos fundamentalmente el ácido zoledrónico que incorporan nitrógeno a su molécula, muestran un efecto inhibidor de la proliferación celular tumoral y de la angiogénesis. Todo lo cual puede contribuir a la inhibición de la resorción ósea y llevar a un incremento de la masa ósea1.
Berenson determinó la eficacia y seguridad del tratamiento con pamidronato y ácido zoledrónico en pacientes con mieloma múltiple. Observó que la infusión de éstos a largo plazo como un tratamiento adyuvante a la quimioterapia era superior a la quimioterapia sola para reducir el número de eventos esqueléticos en los pacientes, mejorando así mismo, la supervivencia2, 3.
Este beneficio observado en mieloma múltiple llevó a la recomendación del uso de pamidronato o ácido zoledrónico de forma indefinida, debiendo ser suspendido este tratamiento sólo en el caso de que surgieran efectos deletéreos4. Los efectos adversos comunes de los bisfosfonatos incluyen síntomas gripales, astenia, reacciones gastrointestinales, anemia, disnea y edema5. En 2003 se comunicó la primera posible asociación entre el tratamiento con bisfosfonatos y la aparición de necrosis avascular del maxilar.
Presentamos el caso de un paciente con mieloma múltiple que desarrolló una osteonecrosis mandibular secundaria al tratamiento con bisfosfonatos.
CASO CLINICO:
Paciente varón de 48 ańos diagnosticado de mieloma múltiple IgA lambda, Bence-Jones positivo, estadio I-A en noviembre de 2003. Como antecedente presentaba asma con moderada obstrucción al flujo aéreo. Se inició tratamiento quimioterápico según esquema VAD (vincristina, adriamicina y dexametasona), recibiendo 4 ciclos y ante la respuesta parcial obtenida, en marzo de 2004 se continuó con 6 ciclos de quimioterapia alternante VBMCP/VBAD (vincristina, carmustina, melfalán, ciclofosfamida y prednisona/vincristina, carmustina, adriamicina y dexametasona),. En la evaluación posterior se objetivo una respuesta parcial en diciembre de 2004, por lo que se inició tratamiento con talidomida hasta dosis de 600 mg/ día y dexametasona 40 mg/día durante 4 días trisemanal. Se desestimó la realización de un trasplante autólogo de sangre periférica por obstrucción severa al flujo aéreo.
Dado que en la serie ósea se observaba osteporosis en el esqueleto axial, en marzo de 2004, se había iniciado tratamiento con ácido zoledrónico a dosis de 4 mg vía endovenosa cada 4 semanas junto con la asociación de Carbonato de Calcio y Colecalciferol oral.
En noviembre de 2005, el paciente presentó un intenso dolor en región submandibular izquierda, objetivándose a la exploración física un absceso en dicha zona y en la exploración de la cavidad oral se apreciaron numerosas caries, falta de varias piezas dentales y un fragmento correspondiente a la rotura del 1ş molar inferior izquierdo. Ante la sospecha de osteonecrosis en relación con bisfosfonato se suspendió dicho tratamiento y se solicitó TAC de macizo facial; así mismo, se pautó tratamiento antibiótico de amplio espectro (Amoxicilina-Ácido Clavulánico), analgésicos y enjuagues con Clorhexidina, junto con una valoración odontológica. En el TAC efectuado sólo se apreciaba un edentualismo parcial y una pequeńa adenopatía submandibular izquierda. El odontólogo recomendó tratamiento conservador.
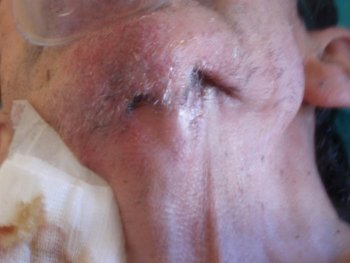
En mayo de 2006, el paciente presentó un nuevo absceso submandibular izquierdo con drenaje espontáneo y aparición de 2 fístulas mandibulares con supuración purulenta continua (figura 1). En las semanas posteriores, se realizaron varios cultivos y se pautó tratamiento antibiótico según el antibiograma.
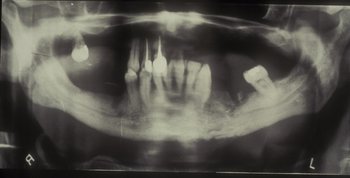
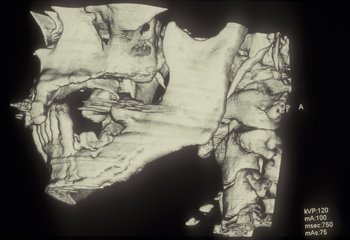
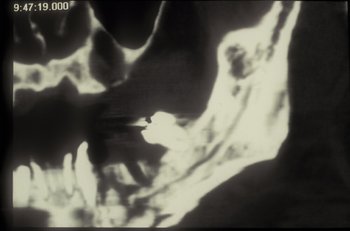
La ortopantomografía solicitada mostraba una imagen lítica en rama mandibular izquierda (figura 2). En el TAC efectuado posteriormente se observaron lesiones compatibles con osteonecrosis mandibular (figuras 3-4): aparecían múltiples imágenes líticas en la rama mandibular izquierda, existiendo múltiples fragmentos aislados así como múltiples líneas que interrumpen la cortical anterior y posterior.
En mayo de 2006 se solicitó valoración por Cirugía Plástica para tratamiento quirúrgico que fue desestimado por insuficiencia ventilatoria obstructiva grave con disminución severa de FVC detectada en la exploración funcional respiratoria. Se suspendió el tratamiento con talidomida ante la progresión del mieloma, y se inició tratamiento con bortezomib y dexametasona; el paciente ha recibido 8 ciclos obteniéndose una respuesta completa con normalización de la paraproteína.
Actualmente, persiste una fístula cutánea que le ocasiona intenso dolor.
DISCUSIÓN
Wang et al6 fueron los primeros en describir este hallazgo en tres pacientes que recibían tratamiento quimioterápico por cáncer de mama; en todas las pacientes se había asociado al tratamiento pamidronato; en dos casos la necrosis apareció tras una extracción dentaria pero en la tercera apareció espontáneamente. En todos los casos el examen histológico de la mandíbula mostró un hueso necrótico sin evidencia de metástasis.
Prácticamente al mismo tiempo apareció otra publicación de Marx describiendo 36 casos de necrosis avascular del maxilar en pacientes que habían recibido pamidronato o ácido zoledrónico. 18 de los pacientes (50%) presentaban un mieloma. La mayoría desarrollaron la complicación tras una extracción dentaria pero hasta en un 30% de los casos apareció de forma espontánea7.
Las primeras revisiones amplias sobre esta complicación fueron la de Marx con 36 casos en 20037, Ruggiero con 63 casos en 20048 y Bagan con 10 casos en 20059. En la serie de Ruggiero de los 63 casos 28 tenían un mieloma. En la de Bagan, de los 10 pacientes afectados, 4 tenían un mieloma.
No se conoce la incidencia real de esta complicación ya que en los estadios iniciales del proceso, los cambios óseos pueden pasar desapercibidos en las pruebas radiológicas1. En estudios retrospectivos se ha observado una incidencia del 9.9% en pacientes con mieloma10.
Este efecto secundario no había sido detectado en los ensayos clínicos por lo que en septiembre de 2004 el laboratorio farmacéutico que comercializa Aredia (pamidronato) y Zometa (ácido zoledrónico) emitió un comunicado incluyendo la necrosis avascular como posible efecto secundario 11.
Esta complicación parece estar causada por una falta de aporte vascular, de remodelado y regeneración ósea. La necrosis ósea avascular se ha descrito localizada únicamente en los maxilares, tanto en el superior como en la mandíbula. La predilección por esta localización podría estar en relación con que los maxilares están constituidos por un tejido óseo sometido a traumatismos continuos y expuesto al medio ambiente a través del surco gingival. Otro factor apuntado en la posible etiología sería que las arterias mandibulares son arterias terminales lo que favorecería la génesis de la osteonecrosis1.
Es interesante destacar que estos pacientes tienen lesiones que recuerdan a aquellas vistas en casos de osteorradionecrosis. Varios autores han propuesto que las propiedades antiangiogénicas de los bisfosfonatos, con la alteración en el metabolismo mediada por la inhibición de los osteoclastos, conduce a una plausible explicación para el desarrollo de la osteonecrosis de mandíbula. De forma similar a los pacientes con osteorradionecrosis, los pacientes tienen expuesto el hueso alveolar necrótico. Sin embargo, a diferencia de ellos los pacientes con osteonecrosis por bisfosfonatos no responden a la terapia con oxígeno hiperbárico. Aunque se ha descrito algún caso de desaparición del dolor con el uso de oxígeno hiperbárico asociado a antibióticos12.
La osteonecrosis de la mandíbula recuerda a la enfermedad profesional llamada "fossy jaw" que se producía en trabajadores de las factorías que usaban fósforo en la manufactura. Esta enfermedad se caracterizaba por un intenso dolor en los maxilares refractario al tratamiento analgésico y por aparición de lesiones desfigurantes 13.
Los bisfosfonatos no son metabolizados y por ello, pueden persistir en el hueso durante meses y a veces ańos tras la discontinuación del fármaco. La suspensión del tratamiento con bisfosfonatos no parece acelerar la recuperación de la osteonecrosis.
El mecanismo subyacente de la reacción es desconocido, pero ha sido postulado que los bisfosfonatos inhiben la formación de nuevos vasos, por ello deterioran la cicatrización. Aunque la extracción dental y la cirugía oral han sido identificadas como precipitantes en muchos casos, hay evidencias que sugieren que el hueso alveolar puede estar afectado antes e independientemente de estos procedimientos. Así, la presentación clínica puede simular perfectamente un absceso dental, dolor de muelas, puntos dolorosos en la dentadura y osteomielitis.
Los síntomas más comunes son dolor (78,8%) seguido de secreción purulenta (8,2%), ulceración (2,3%) y fiebre (1,2%). En el 74% de los pacientes existe el antecedente de una extracción dental en el área afectada14.
El riesgo de osteonecrosis aumenta con la manipulación dental y la mala higiene de tal manera que al exponerse el hueso a la flora tras las extracciones dentarias, se sobreinfecta produciendo dolor, tumefacción y supuración y, finalmente necrosis ósea.
La Fundación Internacional de Mieloma realizó una encuesta durante 2004 para valorar los factores de riesgo de osteonecrosis del maxilar. De los 1.203 casos que se recogieron en la encuesta, 904 tenían un mieloma (75%). De éstos, el 71% habían recibido ácido zoledrónico y el 29% pamidronato sólo; el análisis a los 36 meses mostró que la osteonecrosis se desarrolló en el 10% de los pacientes que recibieron ácido zoledrónico comparado con el 4% de los que recibieron pamidronato. La media de tiempo para la aparición de la complicación fue de 18 meses para el ácido zoledrónico y de 72 meses para el pamidronato. El antecedente de problemas dentales como la infección o la extracción dental aparecía en el 81% de los pacientes con mieloma que desarrollaron osteonecrosis15.
En otro estudio efectuado por el grupo de Dimopoulos, la media de tiempo de la exposición a los bisfosfonatos fue de 39 meses para los pacientes con osteonecrosis. Estos autores describen que el riesgo acumulado para desarrollar este efecto secundario fue significativamente más alto en pacientes tratados con ácido zoledrónico solo que en aquellos tratados con pamidronato solo o pamidronato y posteriormente ácido zoledrónico16.
Existen un aserie de factores de riesgo documentados en el desarrollo de la osteonecrosis entre los que se incluyen tratamiento con quimioterapia, corticoides, talidomida y condiciones de comorbilidad como anemia, coagulopatía, higiene dental defectuosa y enfermedad oral preexistente.
No se ha establecido un tratamiento efectivo; algunos responden a tratamiento antibiótico (amoxicilina asociada a ácido clavulánico) junto con irrigaciones con clorhexidina al 0,12% y desbridación de secuestros óseos1.
Desafortunadamente algunos pacientes pueden llegar a requerir la resección de una parte del maxilar17.
No está claro si la discontinuación del fármaco puede alterar el curso de la osteonecrosis maxilar dado que el fármaco permanece en el hueso durante ańos, pero se recomienda suspender el fármaco para facilitar la recuperación local. Se ha descrito algún caso resuelto tras la discontinuación de la terapia con bisfosfonatos durante 4 meses18.
Dado el aumento en el número de casos comunicados de osteonecrosis del maxilar asociado a bisfosfonatos han surgido varias guías de actuación para la prevención, diagnóstico y tratamiento de esta complicación13.
Puesto que el tratamiento de este efecto secundario es complejo, la principal actuación para evitar su aparición debiera ser la prevención. Esto conlleva que todos los profesionales implicados, especialmente los odontólogos, hematólogos y cirujanos maxilofaciales deben ser conscientes del riesgo de aparición de este efecto en pacientes que reciben bisfosfonatos. También, es importante informar del riesgo de esta complicación a los pacientes.
REFERENCIAS
-
1.- Jimenez-Soriano Y, Bagan JV. Bisphosphonates, as a new cause of drug-induced jaw osteonecrosis: An update. Med Oral Patol Oral Cir Bucal 2005; 10 Suppl 2: E88-91.
2.- Berenson JR, Lichtenstein A, Porter L, Dimipoulos M, Bordoni R, George S, et al. Efficacy of pamidronate in reducing skeletal events in patients with advanced multiple myeloma. N Engl J Med 1996; 334: 488-493.
3.- Berenson JR, Rosen LS, Howell A et al. Zoledronic acid reduces skeletal-related events in patients with osteolytic metastases. Cancer 2001; 91: 1191-1200.
4.- Berenson J. American Society of Clinical Oncology clinical practice guidelines: the role of bisphosphonates in multiple myeloma. J Clin Oncol 2002; 20: 3719-36.
5.- Wellington K, Goa KL. Zoledronic acid: a review of its use in the mangement of bone metastases and hypercalcemia of malignancy. Drugs 2003; 63: 417-437.
6.- Wang J, Goodger NM, Pogrel MA. Osteonecrosis of the jaws associated with cancer chemotherapy. J Oral Maxillofac Surg 2003; 61: 1104-7.
7.- Marx RE. Pamidronate (Aredia) and Zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemia. J Oral Maxillofac Surg 2003, 61: 1115-8.
8.- Ruggiero S Mebrotra B, Rosenberg T, Enggroff S. Osteonecrosis of the jaws associated with the use of bisphosphonates: a review of 63 cases. J Oral Maxillofac Surg 2004; 62: 527-534.
9.- J. V. Bagan, J. Murillo, Y. Jiménez, R. Poveda, M. A. Milian, J. M. Sanchis, F. J. Silvestre, C. Scully. Avascular jaw osteonecrosis in association with cancer chemotherapy: series of 10 cases. J Oral Pat Med 2005; 34: 120.
10.- Bamias A, Kastritis E, Bamia C et al. Osteonecrosis of the jaw in cancer alter treatment with bisphosphonates: incidente and risk factors. J Clin Oncol 2005; 23:8580-7.
11.- Changes to the precautions and post-marketing experience sections of Aredia (pamidronate disodium) injection and Zometa (zoledronic acid) injection prescribing information related to osteonecrosis of the jaw. September 24, 2004 (pakningsvedlegg) http://www.novartis.com (16.6.2005). Ver http://www.fda.gov/medwatch/SAFETY/2004/ZometaHCP.pdf (12.12.2006)
12.- Shimura K, Shimazaki C, Taniguchi K, Akamatsu S, Okamoto M, Uchida R, Nomura K, Inaba T, Horiike S, Kanamura N, Taniwaki M. Hyperbaric oxygen in addition to antibiotic therapy is effective for bisphosphonate-induced osteonecrosis of the jaw in a patient with multiple myeloma. Int J Hematol. 2006; 84: 343-5.
13.- Lacy MQ, Dispenzieri A, Gertz MA, Greipp R, Gollbach KL, Hayman SR, Kumar S, Lust JA, Rajkumar SV, Russell SJ, Witzig TE, Zeldenrust SR, Dingli D, Bergsagel PL, Fonseca R, Reeder CB, Stewart K, Roy V, Dalton RJ, Carr AB, Kademani D, Keller EE, Viozzi CF, Kyle RA. Mayo clinic consensus statement for the use of bisphosphonates in multiple myeloma. Mayo Clin Proc. 2006 ;81: 1047-53.
14.- Van der Wyngaer T, Huizing M, Vermorken J et al. Biphosphonates and osteonecrosis of the jaw. Eur J Cancer 2005; 3: 363.
15.- Durie B. Osteonecrosis of the Jaw and Bisphosphonates. NEJM; 2005; 353: 99-102.
16.- Dimopoulos MA, Kastritis E, Anagnostopoulos A, Melakopoulos I, Gika D, Moulopoulos LA, Bamia C, Terpos E, Tsionos K, Bamias A. Osteonecrosis of the jaw in patients with multiple myeloma treated with bisphosphonates: evidence of increased risk after treatment with zoledronic acid. Haematologica. 2006; 91: 968-71.
17.- Kademani D, Koka S, Lacy MQ, Rajkumar SV. Primary surgical therapy for osteonecrosis of the jaw secondary to bisphosphonate therapy. Mayo Clin Proc. 2006; 81: 1100-3.
18.- Migliorati CA, Schubert MM, Peterson DE, Seneda LM. Bisphosphonate-associated osteonecrosis of mandibular and maxillary bone: an emerging oral complication of supportive cancer therapy. Cancer. 2005; 104: 83-93.
En este artículo describe un caso clínico de un paciente que desarrolló una osteonecrosis del maxilar después de llevar unos 20 meses de tratamiento con ácido zoledrónico y que progresó a pesar de interrumpir el tratamiento. También se discute el mecanismo por el que se puede producir este efecto adverso.
Comentario del revisor Prof. Francisco Abad Santos. Servicio de Farmacología Clínica. Hospital la Princesa. Departamento de Farmacología y Terapéutica de la Facultad de Medicina. Universidad Autónoma de Madrid. Espańa
Los pacientes con mieloma múltiple suelen requerir tratamiento con bifosfonatos potentes de forma prolongada para evitar las lesiones osteoesqueléticas. Estos fármacos suele ser bien tolerados por la mayoría de los pacientes, pero en algunos casos puede aparecer un efecto adverso grave que se ha descrito en los últimos ańos.
Comentario del revisor María Jesús Coma del Corral. Responsable de la Unidad de Investigación del Hospital General Yagüe de Burgos. Espańa. Editora.
Los autores presentan un nuevo caso de osteonecrosis del maxilar en paciente con mieloma múltiple tratado con bisfosfonatos, una complicación que está empezando a manifestarse con relativa frecuencia, avlado por una magnífica iconografía.
Como detalla el editorial que acompańa a este mismo número de Rev Electron Biomed, el efecto secundario que describe este artículo, no fue detectado en los ensayos clínicos que fueron realizados en su día, siendo apreciado posteriormente cuando el número de pacientes sometidos a tratamiento fué considerable. Este artículo por tanto, es tambien una llamada de atención a la necesidad de realizar ensayos clínicos suficientes, tambien los postcomercialización así como esmerar la farmacovigilancia.
Recibido, 18 de noviembre de 2006. Recibido revisado, 21 de Diciembre de 2006
Publicado, 23 de Diciembre de 2006