Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
- Cada ańo 2.2 millones de pacientes hospitalizados sufren una reacción adversa grave.
- Las reacciones adversas constituyen entre la cuarta y la sexta causa de muerte en los Estados Unidos.
- Las admisiones hospitalarias debido a reacciones adversas ocupan más del 10% en algunos países.
- Más del 20% del presupuesto de salud es empleado en complicaciones producidas por fármacos.
- Desde 1995 el costo asociado a los problemas relacionados con los medicamentos se ha duplicado.
REACCIONES ADVERSAS A MEDICAMENTOS EN UNA UNIDAD DE TERAPIA INTENSIVA.
Ismary Alfonso Orta MD, Odalys Garcia Arnao MSc**, Alfredo Triolet Galvez MD**, Carmen Gómez MD**, Karelia Ruiz MD***
*Centro para el Desarrollo de la Farmacoepidemiología (CDF). **Hospital Calixto García Ińiguez.
*** FCMH: Calixto García. Ciudad Habana. Cuba
isma.alfonso @ infomed.sld.cu
Rev Electron Biomed / Electron J Biomed 2008;2:10-18
Comentario del revisor Prof. Enrique Seoane-Vázquez Ph.D. Assistant Professor. College of Pharmacy and College of Public Health. The Ohio State University. Columbus. USA.
Comentario del revisor Dª. Blanca de la Nogal Fernández. Servicio de Farmacia. Hospital General Yagüe. Burgos. Espańa
ABSTRACT:
Introduction: Pharmacovigilance is a public health for the identification, evaluation and prevention of risks associated with drugs once marketed. They constitute a major health problem in fact in some developed countries adverse drug reactions that lead to admission to emergency services constitute a major cause of death, preceded only by ischemic heart disease, cancer and stroke. Our research suggested the study of the behavior of adverse drug reactions (ADRs) reported in the intensive therapy unit (ICU) of the Hospital Calixto García from the year 2000 to 2005.
Method: A study of Pharmacovigilance Hospital retrospective and descriptive using the methods of notification Spontaneous adverse reactions and intensive monitoring of patients admitted to the service of intensive therapy unit of University Hospital "General Calixto García Ińiguez" of Havana which consisted in the analysis of adverse drug reactions reported in the period from 2000 until 2005.
Results: We detected 277 adverse drug reactions in 119 notifications of patients. The drug associated with an increased number of notifications recombinant streptokinase was 61.3%. More than 50% of RAM detected affected systems: cardiovascular, gastrointestinal, general declarations. Predominated moderate adverse reactions (43.3%) although the grave were present in addition 36.8% 3 fatal cases (1.08%) 86.3% of them were classified as probable.
Conclusions: Were detected between two or three adverse drug reactions for each notification. Leaving clear the high responsibility for selecting treatment in these patients, streptokinase was the drug most commonly associated with adverse reactions reported, the digestive system was the most affected and adverse reactions that predominated were moderate and probable. We need to monitor selected drugs as well as notify serious or unexpected reactions that may occur.
Keywords: Pharmacovigilance hospital, Adverse Drug Reactions, adverse effects
RESUMEN
La farmacovigilancia es una actividad de Salud Pública destinada a la identificación, evaluación y prevención de los riesgos asociados a los medicamentos una vez comercializados. Constituyen un problema sanitario importante de hecho en algunos países desarrollados las reacciones adversas a medicamentos que dan lugar a ingreso en servicios de urgencia constituyen una de las principales causas de muerte, sólo precedidas por la cardiopatía isquémica, el cáncer y el accidente cerebrovascular. Nuestra investigación se propuso conocer el comportamiento de las reacciones adversas medicamentosas (RAM) notificadas en la Unidad de Terapia Intensiva (UTI) del Hospital Calixto García desde el ańo 2000 hasta 2005.
Método: se realizó un estudio retrospectivo y descriptivo utilizando los métodos de Notificación Espontánea de Reacción Adversa y la monitorización intensiva de Pacientes Ingresados en la Unidad de Terapia Intensiva del Hospital Universitario "General Calixto García Ińiguez" de Ciudad de la Habana, que consistió en el análisis de las reacciones adversas a medicamentos notificadas en el periodo comprendido desde el ańo 2000 hasta el 2005.
Resultados: se detectaron 277 reacciones adversas a medicamentos en 119 notificaciones de pacientes. El fármaco asociado a un mayor numero de notificaciones (61.3%), fue la estreptoquinasa recombinante. Más del 50% de la RAM detectadas afectaron los sistemas cardiovascular, digestivo, o bien fueron manifestaciones generales. Predominaron las reacciones adversas moderadas (43.3%) aunque las graves estuvieron presentes en el 36.8% de losc asos. Además hubo 3 casos mortales (1.08%). El 86.3% de las RAM se clasificaron como probables.
Conclusiones: se detectaron entre dos o tres reacciones adversas a medicamentos por cada notificación realizada. Dejando claro la elevada responsabilidad a la hora de seleccionar el tratamiento en este tipo de pacientes, la estreptoquinasa fue el fármaco más asociado a las reacciones adversas notificadas, el sistema digestivo fue el más afectado y las reacciones adversas que predominaron fueron las moderadas y probables. Hay que monitorizar los fármacos seleccionados así como notificar las reacciones graves o inesperadas que puedan ocurrir.
Palabras Clave: Farmacovigilancia Hospitalaria, Reacciones adversas a medicamentos, Efectos adversos.
INTRODUCTION
La farmacovigilancia es una actividad de salud pública destinada a la identificación, evaluación y prevención de los riesgos asociados a los medicamentos una vez comercializados1-2. La incidencia de reacciones adversas medicamentosas (RAM) encontrada en diversos estudios varía entre el 1% y el 30% como resultado de las diferentes metodologías empleadas para detectar y evaluar estas reacciones, los estilos diferentes de prescripción de medicamentos y la inclusión o exclusión de las reacciones leves. Sin embargo la mayoría de los estudios prospectivos muestran que la incidencia de RAM en los pacientes hospitalizados (excluyendo los pacientes con reacciones leves) es entre el 10% y el 20%3-4.
Se considera reacción adversa como: "reacción nociva y no intencionada que se produce a dosis utilizadas normalmente en el hombre para la profilaxis, el diagnóstico, el tratamiento de enfermedades o para la modificación de una función fisiológica" (OMS, 1972).
El uso extendido del medicamento establece el alcance definitivo de los riesgos (efectos adversos) y de los beneficios (eficacia terapéutica) en sus diferentes indicaciones terapéuticas; dejando en evidencia la importancia de la farmacovigilancia para controlar el comportamiento del medicamento una vez que ha sido aprobado para su uso por la autoridad sanitaria5.
Una gran proporción de las RAM se deben a un uso no racional de los medicamentos o a errores humanos, y por consiguiente son evitables. Las principales causas son: diagnóstico erróneo, prescripción del medicamento equivocado o de una dosis equivocada del medicamento correcto, trastornos médicos, genéticos o alérgicos subyacentes causantes de la RAM, automedicación, incumplimiento del tratamiento prescrito, interacciones entre medicamentos en pacientes tratados con múltiples fármacos. Las reacciones adversas producidas por los medicamentos constituyen un problema sanitario importante. De hecho en algunos países desarrollados los efectos indeseables que dan lugar a ingreso en servicios de urgencia constituyen una de las principales causas de muerte, sólo precedidas por la cardiopatía isquémica, el cáncer y el accidente cerebrovascular6-7.
La admisión de pacientes a los hospitales por causa de reacciones adversas a medicamentos es relativamente común. Varios estudios han mostrado que entre el 3% y el 7% de los pacientes son admitidos a los hospitales debido a reacciones adversas. Alrededor del 10% al 20% de las RAM en pacientes hospitalizados son graves. Las muertes inducidas por medicamentos son raras y ocurren en el 0.5% y el 0.9% de los pacientes hospitalizados8-10.
Los reportes epidemiológicos relacionados con las reacciones adversas medicamentosas hablan por si mismos de la extraordinaria importancia de esta temática, por solo citar algunos datos2:
A mediados de los ańos sesenta se comenzaron a probar métodos de farmacovigilancia que pudieran complementar la notificación espontánea de sospechas de RAM, razón por la cual surge la monitorización o supervisión intensiva de pacientes hospitalizados, método fiable para detectar efectos indeseables por fármacos amén de sus desventajas y/o limitaciones11-12.
Las reacciones adversas evitables también denominadas en la literatura "acontecimientos adversos por medicamentos (AAM) prevenibles", que son los causados por errores de medicación, ocasionaban en EE.UU. más de 7.000 muertes anuales, cifra que supera a las causadas por los accidentes de trabajo. Según los resultados del ADE Prevention Study, casi un 2% de los pacientes en el medio hospitalario presenta AAM prevenibles durante su estancia, hecho que incrementa el costo medio del ingreso en 4.700 dólares, lo que extrapolado a la totalidad de EE.UU. supone un costo anual de dos mil millones de dólares13.
Por todo lo antes expuesto el propósito de nuestra investigación es conocer el comportamiento de las sospechas de reacciones adversas medicamentosas (RAM) notificadas en la Unidad de Terapia Intensiva (UTI) del Hospital Calixto García desde el ańo 2000 hasta 2005, sumado a identificar los grupos de pacientes según sexo y edades en los cuales ocurrieron sospechas de RAM, conocer cuales fueron los fármacos sospechosos de producir RAM, analizar y clasificar las Sospechas de RAM notificadas.
PACIENTES Y METODOS
Se realizó un estudio de Farmacovigilancia Hospitalaria retrospectivo y descriptivo utilizando los métodos de Notificación Espontánea de Sospecha de Reacción Adversa y la monitorización de Pacientes Ingresados en el servicio de UTI del Hospital Universitario "General Calixto García Ińiguez" de Ciudad de la Habana que consistió en el análisis de las RAM notificadas en el periodo comprendido desde el ańo 2000 hasta el 2005.
La información fue obtenida por revisión de historias clínicas y el modelo oficial de notificación de sospechas de RAM emitido por el Ministerio de Salud Pública de Cuba.
Se determinó la distribución por sexo y por edades (15-30, 31-60 y mayores de 60 ańos). La clasificación de las RAM fue realizada por el grupo de expertos de farmacovigilancia del hospital, discutiendose de manera individualizada cada caso notificado, uniformidad en las opiniones y criterios de los expertos. Se clasificaron siguiendo los criterios de causalidad por el algoritmo de Karch y Lasagna, que agrupa las reacciones en definitivas, probables, posibles, condicionales o no relacionadas14.
Según grado de severidad se clasificaron como leves: cuando los síntomas y signos fácilmente tolerados, no requieren cambio de terapéutica ni antidoto terapia. Moderadas: cuando hay malestar suficiente que interfiere con la actividad usual, éstas requirieron observación o cambio de terapéutica y no necesariamente se precisó la suspensión del fármaco. Graves: cuando pusieron en peligro la vida del paciente y por tanto requirieron la suspensión del fármaco causante de la reacción y la administración de un tratamiento específico para contrarrestarla. Letales: cuando contribuyeron directa o indirectamente a la muerte del paciente14.
Según criterios de Rawlins y Thompson 15
A (augmented): predecibles o al menos esperables (relacionada con sus acciones farmacológicas). La intensidad de la respuesta se relaciona con la dosis administrada. Su tratamiento requiere ajuste de la dosis.
B (bizarre): son reacciones raras, no predecibles a priori por las propiedades farmacológicas de un medicamento administrado a las dosis terapéuticas habituales. No existe relación entre la dosis y la intensidad de la reacción. Probable mecanismo inmunológico o genético.
C (chronic): asociadas a tratamientos prolongados.
D (delayed): son las retardadas (carcinogénesis y teratogénesis).
Las manifestaciones clínicas se agruparon por órganos/sistemas utilizando la terminología empleada por la OMS16 y finalmente se identificaron los fármacos mayormente implicados en la aparición de efectos indeseables.
Se utilizó estadística descriptiva para el análisis de los objetivos.
RESULTADOS
Se detectaron 277 sospechas de Reacciones Adversa a medicamentos en 119 notificaciones realizadas Las tablas 1 y 2 muestran como las sospechas de RAM predominaron en el sexo masculino (54.6%), y en las edades entre 31 y 60 ańos (53.8%). De hecho el infarto agudo del miocardio (IMA) fue la indicación que con mayor frecuencia motivó la administración de fármacos causantes de efectos indeseables (61.3 %).
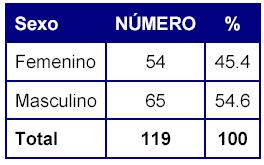
Tabla 1: Distribución de las sospechas de RAM según el sexo
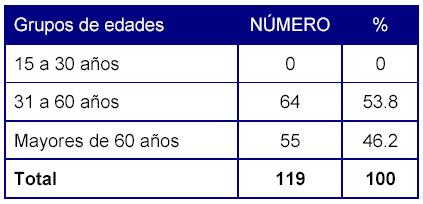
Tabla 2: Distribución de las sospechas de RAM según grupos etáreos.
En la tabla 3 se muestran los fármacos sospechosos de producir RAM en pacientes ingresados en la UTI donde podemos citar en primer lugar a la Estreptoquinasa Recombinante (fibrinolítico) responsable del 61.3% de los eventos, además de otros como antibióticos, Intacglobin, Digoxina, Heparina, con menos proporción de casos.
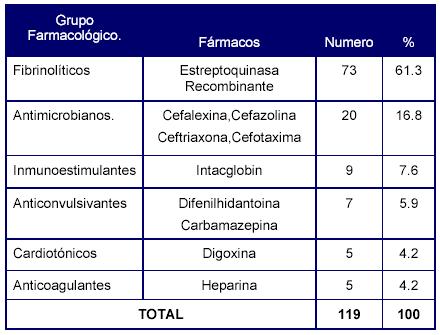
Tabla 3: Distribución de los fármacos sospechosos de producir las sospechas de RAM.
Entre las reacciones adversas detectadas las más frecuente fueron los trastornos gastrointestinales (22.4%), seguido de los escalofríos (18.8%) y la hipotensión arterial (15.8%) derivada en un 100 % de la Estreptoquinasa, que en todos los casos al aplicarle el algoritmo de Karch-Lasagna (causalidad) se consideraron posibles, pues la patología de base podría ser causa que explicara la reacción adversa (Tabla 4) También se recogieron otras reacciones como arritmias, hipersensibilidad, hemorragias, trastornos del sistema nervioso central.
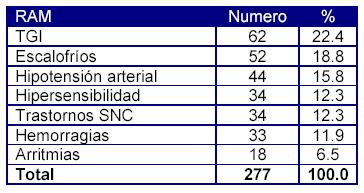
Tabla 4: Distribución de las sospechas de RAM notificadas según su tipo.
La tabla 5 muestra el comportamiento según severidad, donde se observa que las reacciones más frecuentes en nuestro estudio fueron las reacciones moderadas (43.3%). Nada despreciable fue el número de reacciones graves que se detectaron (36.8%).
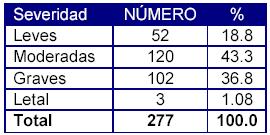
Tabla 5: Distribución de las sospechas de RAM notificadas según su severidad.
Tuvimos además tres reacciones letales (1.08%). Las RAM letales fueron una hemorragia cerebral fatal la cual al aplicar el algoritmo de causalidad clasifico como probable, debida a la utilización de Estreptoquinasa Recombinante en un Infarto Agudo del Miocardio (IMA), una hipotensión arterial y una arritmia ventricular ambas imputadas como posibles por la utilización del mismo fármaco en la misma indicación.
Al aplicar el algoritmo de Karch y Lasagna la casi totalidad de las reacciones fueron catalogadas como probables (86.3%) y posibles (13.7%), demostrando en este último caso que el cuadro clínico de la RAM podía obedecer también a otra causa, además del medicamento del que se sospechaba la reacción (tabla 6).
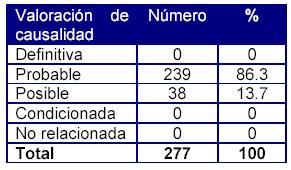
Tabla 6: Distribución de las sospechas de RAM según el algoritmo de Karch y Lasagna.
Las reacciones tipo A por la clasificación de Rawlins y Thompson fueron las de mayor cuantía (87.7%). No predecibles fueron 34 sospechas de RAM de hipersensibilidad. Los vómitos bastaron por sí solos para situar al aparato digestivo como uno de los más afectados.
DISCUSION
Debemos tener en cuenta que en este tipo de servicio se facilita la supervisión estrecha del paciente, expuesto generalmente a un número considerable de medicamentos, lo que pudiera predisponer incluso a la aparición de RAM por interacciones medicamentosas. Además el método de monitorización intensiva no posee riesgo de infranotificación que si pudiera presentarse con el método de la notificación espontánea.
Los resultados encontrados en la distribución de las reacciones adversas según sexo y grupo de edades difieren de lo consultado en la literatura ya que se plantea que existe una mayor frecuencia de aparición de RAM en el sexo femenino, e incluso para algunos autores este constituye un factor de riesgo que puede propiciar la aparición de una RAM17, pero igualmente justificable por las características del servicio, que admite fundamentalmente portadores de enfermedades cardíacas, más frecuentes en hombres que en mujeres17, y con elevada prevalencia en los menores de 65 ańos18-19.
Se corresponde también otros con estudios nacionales la proporción de fármacos sospechosos de producir RAM en pacientes ingresados en la UTI donde podemos citar en primer lugar a la Estreptoquinasa Recombinante que represento el fármaco asociado a mayor numero de notificaciones20. Las reacciones adversas notificadas en el estudio mostraron un comportamiento similar a un estudio realizado en otro hospital de nuestro país ańo 2005 destacando de igual forma vómitos, bradicardia, hipotensión y extrasístoles20.
Al analizar el mecanismo mediante el cual la estreptoquinasa produjo la hipotensión arterial conocemos que no está bien establecido y nos inclinamos por uno de los tantos propuestos, relacionado con la dosis del medicamento que pasa en un minuto durante la hora que dura la infusión21-22. Y lo hacemos teniendo en cuenta que en nuestro estudio la mayoría de los pacientes que presentaron esta reacción mejoraron con la sola disminución del goteo. En otros si fue preciso suspender la medicación pues hubo compromiso hemodinámico importante.
A pesar de que todas las publicaciones nacionales e internacionales coinciden en que son las reacciones leves las que con mayor frecuencia aparecen 1, 20, en nuestro estudio predominaron las reacciones moderadas (43.3%), como se expuso en la tabla 5. Tuvimos además tres reacciones letales (1.08 %), cifra que se incluye dentro del rango referido por la literatura23. Tal y como se recoge en la bibliografía6, 13 las reacciones tipo A por la clasificación de Rawlins y Thompson fueron las más frcuentes (87.7%), de ahí que en múltiples ocasiones se minimizaran los efectos realizando simples ajustes de dosis.
El predominio de reacciones adversas moderadas y un numero nada despreciable de graves se justifica por el estado en que se encuentran los pacientes que ingresan en unidades de cuidados intensivos los hace más susceptibles de descompensaciones hemodinámicas o de otro tipo, que pueden interferir en su recuperación o incluso llegar a comprometer su vida.
El resultado mostrado según causalidad pone de manifiesto algunas de las limitaciones de los algoritmos a la hora de establecer la relación de causalidad entre una supuesta reacción adversa y el medicamento sospechoso de producirla. Así por ejemplo, en nuestro estudio hubo sospechas de RAM que pudieron ser clasificadas como máximo de probables y no como definitivas, aún en ausencia de otras causas alternativas inmediatas. Sucede que para que una sospecha sea catalogada como una RAM definitiva además de manifestarse con una secuencia temporal plausible en relación con la administración del medicamento, y de no poder explicarse por una enfermedad concurrente ni por otros fármacos o sustancias, tiene que aparecer necesariamente tras la reexposición24, y esto sin lugar a dudas implica un cuestionamiento ético por parte del médico, que debe tener como principio básico no hacer dańo.
Como hemos podido apreciar en el transcurso de la discusión la estreptoquinasa fue el fármaco responsable de la mayor cantidad y variedad de efectos indeseables detectados. Si aún quedaran dudas al respecto, podríamos citar entonces las complicaciones hemorrágicas que se presentaron tras su administración, y que contribuyeron a que las hemorragias se ubicaran dentro de las RAM más reportadas . Resulta alentador el que no haya sido tan frecuente como se describe para este tipo de medicamento22, entre otras cosas debido a una buena selección por el personal de la UCI de los pacientes sometidos a tratamiento con fibrinolíticos.
Más del 50% de la RAM detectadas afectaron los sistemas: cardiovascular, digestivo, manifestaciones generales. Estos resultados no guardan gran similitud con los reportados por la Unidad Coordinadora Nacional de Farmacovigilancia en su caso priman las reacciones que afectan la piel y las gastrointestinales, debemos considerar que la mayoría de las notificaciones que se reciben en este centro provienen de la atención primaria de salud, a diferencia de nuestro estudio donde se analizaron reacciones detectadas en una unidad de cuidados intensivos, en la que se emplean fármacos que potencialmente pueden inducir una gran cantidad y/o variedad de manifestaciones cardiovasculares. Sólo la estreptoquinasa de uso exclusivamente hospitalario puede producir hipotensión arterial, bradiarritmias, taquiarritmias extrasístole ventricular moderada hasta una fibrilación ventricular grave 10-13,20,22.
Con respecto a los vómitos este resultado se ha hecho prácticamente una constante en los estudios de farmacovigilancia, y se explica porque la mayoría de los fármacos producen trastornos gastrointestinales, incluso usados por vía parenteral10. Las manifestaciones generales también se ubicaron dentro de las más afectadas, siendo representadas por un grupo amplio de acontecimientos clínicos tales como escalofríos secundarios al uso de la estreptoquinasa y fiebre inducida por intacglobin. Todas reportadas en la literatura como RAM frecuentes tras la administración de estos fármacos25.
CONCLUSIONES:
Se detectaron dos a tres sospechas de RAM por cada notificación realizada. Predominaron en el sexo masculino y en el grupo comprendido entre los 31 a 60 ańos de edad.
Las reacciones adversas mas frecuentes fueron los trastornos gastrointestinales, seguidos de escalofríos y de hipotensión arterial. Predominaron las reacciones moderadas, y probables.
El fármaco de mayor relación con la aparición de RAM fue Estreptoquinasa, así como la patología mas frecuente fue el IMA.
REFERENCIAS
- 1. Buenas Prácticas de Farmacovigilancia del Sistema Espańol de Farmacovigilancia. Ministerio de Sanidad y Consumo. Centro de publicaciones. Madrid 2000.
2. Viewpoint. Parte 1. Vigilando hacia medicinas más seguras. Uppsala Monitoring Centre 2003.
3. Moore N, Lecointre D, Noblet C, Mabille M. Frecuency and cos of serious adverse reactions in a department of general medicine. Br J Clin Pharmacol 1998; 45: 301-8.
4. Pouyanne P, Haramburu f, Imbs l, Beagud B. Admission to hospital caused by adverse drug reactions : cross sectional incidence study. BMJ 2000; 320:1036.
5. Valsecia M. Farmacovigilancia y mecanismos de reacciones adversas a medicamentos. Disponible en: http://med.unne.edu.ar. Fecha de acceso Abril 2007.
6. Otero MJ, Bajo A, Maderuelo JA, Domínguez-Gil A. Evitabilidad de los acontecimientos adversos inducidos por medicamentos detectados en un Servicio de Urgencias. Rev Clin Esp 1999; 199: 796-805.
7. Instituto Catalán de Farmacología. Efectos indeseados: un costo no solo económico. Butlletí groc 1999; 12(1):1-3.
8. Jiménez L G, Debesa G F, Avila P J, Bastanzuri V T. Comportamiento de las reacciones adversas a los analgésicos y antiinflamatorios no esteroideos notificados por el sistema cubano de farmacovigilancia. Primer semestre del ańo 2001. Boletin Fármacos 2002; 5 (2): 1-4.
9. Debesa G F, Jiménez L G, Pérez P J. Vigilancia farmacológica en Cuba. Situación actual. Boletín Fármacos 2001, 4 (1): 1-5.
10. Lazarou J, Pomeranz BH, Corey PN. Incidence of adverse drug reactions in hospitalized patients. A metanalysis of prospective studies. JAMA 1998; 279: 1200-5
11. Laporte JR. Farmacovigilancia en el hospital. En: Laporte JR, Tognoni G, ed. Principios de epidemiología del medicamento. Barcelona: Ediciones Masson-Salvat, 1993: 219-229.
12. Singer K. Adverse drug reactions: current issues and strategies for prevention and management. Expert opinion in pharmacotherapy 2002; 3: 1289-1300.
13. Otero-López M J, Alonso H P, Maderuelo F JA, Garrido C B, Domínguez G A, Sánchez R A. Acontecimientos adversos prevenibles causados por medicamentos en pacientes hospitalizados. Med Clin (Barc). 2006; 126: 81-87.
14. Naranjo CA, Busto UE. Reacciones adversas a medicamentos. En: Naranjo CA, ed. Métodos de farmacología clínica. Toronto: El Service Science, 1992: 330-348.
15. Gruchalla RS. Clinical assessment of drug-induced disease. The Lancet 2000; 356 (9240): 1505-11.
16. The Uppsala Monitoring Centre. Adverse Reaction Terminology, 2000.
17. Pérez JR. Reacciones adversas a medicamentos en pacientes hospitalizados en la Unidad de Cuidados Intensivos. [Trabajo para optar por el título de especialista de I Grado en Medicina Interna]. 2000. Hospital Julio Trigo. Ciudad de la Habana.
18. Rogers WJ. Enfermedad coronaria. En Bennett JC, Plum F, eds. Tratado de Medicina Interna de Cecil. Mexico : Editorial McGraw-Hill Interamerican, 1998: 334-344.
19. Roca R. Temas de Medicina Interna. 4 ed. La Habana. ECIMED, 2002
20. Salazar LE. Reacciones adversas a medicamentos en pacientes hospitalizados en una unidad de cuidados intensivos. Revista Cubana de Medicina Intensiva y Emergencias 2005;4:2-3
21. Goodman and Gilman. Las bases farmacológicas de la terapéutica. 9 ed. México. Editorial McGraw-Hill Interamericana, 1996.
22. Jiménez G. Vigilancia farmacológica de la Estreptoquinasa Recombinante en el tratamiento del Infarto Agudo del Miocardio [Trabajo para optar por el título de especialista de I Grado en Farmacología]. 1999. Hospital Calixto García. Ciudad de la Habana.
23. Madurga M, de Abajo FJ. Farmacovigilancia. En: García AG. INTERCON 96. Indice de especialidades farmacéuticas. Prescripción racional de fármacos. Madrid: Editores Médicos S.A. EDIMSA;1996:160-1.
24. The Uppsala Monitoring Centre. Vigilancia de la seguridad de los medicamentos. Guía para la instalación y puesta en funcionamiento de un centro de farmacovigilancia 2001: 1-24.
25. Colec. de autores. Formulario nacional de medicamentos. Centro para el desarrollo de la Fármaco epidemiología. MINSAP. Editorial Ciencias Médicas. Cuba. 2006. disponible en: http://www.cdf.sld.cu/completo.pdf
Correspondencia:
Dra. Ismary Alfonso Orta
Centro para el Desarrollo de la Farmacoepidemiología (CDF). Ciudad Habana. Cuba
isma.alfonso @ infomed.sld.cu
El articulo de Alfonso Orta y col. es un estudio fármacoepidemiológico que colabora al conocimiento de los riesgos de la utilización de los medicamentos, específicamente las reacciones adversas a los medicamentos.
Los autores presentan una serie de casos de reacciones adversas a medicamentos identificados en la unidad de cuidados intensivos de un hospital cubano que permiten identificar problemas con la utilización de diferentes fármacos, en particular con la estreptoquinasa.
El valor del artículo descansa en su aportación al conocimiento de los problemas de seguridad de los medicamentos de alto uso que derivan en atención en la unidad de terapia intensiva. Éste nuevo conocimiento debe ser considerado en la toma de decisiones relativas a la utilización y monitorización de los medicamentos.
Las unidades de cuidados intensivos son servicios donde, por las
características del paciente atendido así como por los tratamientos
fármaco terapéuticos utilizados (con alto número de principios activos
potentes), es imprescindible hacer un seguimiento exhaustivo de la
evolución del paciente, valorando los efectos tanto deseados como
secundarios o imprevisibles que puedan producir los medicamentos.
Es necesario recordar que la farmacovigilancia es un deber de salud
pública, con el objetivo de una utilización más segura de los
medicamentos.
Al tratarse de una publicación on-line, adjunto dos direcciones de
Internet que me parecen muy interesantes: se puede acceder a las páginas web de los distintos centros de farmacovigilancia existentes en Espańa (descentralizados por Comunidades Autónomas): http://www.icf.uab.es/farmavigila/websefv_e.htm. Otra página que considero muy interesante es la del Instituto Espańol
para el uso seguro de medicamentos, situado físicamente en Salamanca:
http://www.ismp-espana.org/
Comentario del revisor Prof. Enrique Seoane-Vázquez Ph.D. Assistant Professor. College of Pharmacy and College of Public Health. The Ohio State University. Columbus. USA.
Comentario del revisor Dª. Blanca de la Nogal Fernández. Servicio de Farmacia. Hospital General Yagüe. Burgos. Espańa
Recibido: 16 de diciembre de 2007. Recibido revisado: 30 de abril de 2008
Publicado: 20 de junio de 2008
