Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
EFICACIA Y EFECTOS ADVERSOS DEL TRATAMIENTO CON IMIQUIMOD EN LA MUJER CON CONDILOMAS VULVOPERINEALES
Ángel García Iglesias, Silvia García Valle, Miguel Gauro,
Joaquín López Marcos, Tomás Rodríguez Bravo, Consuelo Crespo Martínez, Rafael Collazos Robles.
Departamentos de Obstetricia y Ginecología, Farmacia y Cirugía.
Facultad de Medicina y Hospital Clínico Universitario.
Salamanca. Espańa
aiglesias @ usal.es
Rev Electron Biomed / Electron J Biomed 2010;3:34-41
Comentario del revisor Dra. Esther Martín Sáez. Servicio de Dermatología. Hospital Santiago Apóstol. Miranda de Ebro (Burgos). Espańa.
Comentario del revisor Dra. Lorea Bagazgoitia. Servicio de Dermatología. Hospital Ramón y Cajal. Madrid. Espańa.
ABSTRACT
The genital warts constitute a benign process which appears on young people and it is produced by the HPV. In the course of several years different technics have been used with the goal of settling these kinds of lesions in a fast and safe way.
Aim: To assess the response of the treatment of vulvo-perineal condylomas treated with 5% Imiquimod and the adverse events arised from its use.
Material and methods: The studied population is constituted by 112 patients who presented vulvo-perineal condylomas. Pregnant and HIV positive patients were not included. All of them underwent a complete gynecological study and specifically, cytology, colposcopy, a PCR for HPV and a vulvoscopy to assess the location of the condylomas, size and number of such. Lesions were treated with Imiquimod 5% in cream at alternate nights. Tests were carried out to verify the results of the treatment at 4, 8, 12 and 16 weeks. The maximum time of application was 16 weeks.
Results: The multiple locations were the most common, followed by those ones of the perineal area and the ano-fourchette. The disappearance of condylomas occurred in the highest percentage between 4 and 8 weeks of treatment, and 3 months later no lesions were 88.8%. 87,5% had no lesions at 6 months.The most common side effects were erythema and pruritus.
Conclusions: In view of the results, the treatment with 5% Imiquimod can be considered as an alternative to other destructive therapies, which in turn, acts on the latent infection.
Keywords: Imiquimod. Genital warts. Efficacy. Adverse events.
RESUMEN
Las verrugas genitales constituyen un proceso benigno que aparece principalmente en los jóvenes y que está producido por el virus del papiloma humano. A lo largo de los ańos se han utilizado distintas técnicas con la finalidad de resolver de forma rápida y segura este tipo de lesiones.
Objetivo: valorar la respuesta del tratamiento de los condilomas vulvo-perineales con Imiquimod al 5% y los efectos adversos derivados de su utilización.
Material y métodos: la población estudio está constituida por 112 pacientes que presentaban condilomas vulvo-perineales. No se incluyeron pacientes gestantes ni VIH positivas. A todas ellas se les realizó un estudio ginecológico completo y específicamente, citología, colposcopia, PCR para HPV y vulvoscopia para valorar la localización de los condilomas, tamańo y número de los mismos. Se les pautó tratamiento con Imiquimod al 5% en crema, aplicado en las lesiones a noches alternas. Se realizaron controles para verificar los resultados del tratamiento a las 4, 8, 12 y 16 semanas. El tiempo máximo de aplicación fueron 16 semanas.
Resultados: las localizaciones múltiples fueron las más frecuentes, seguidas de la zona perineal y de la horquilla vulvar. La desaparición de los condilomas se produjo en el mayor porcentaje entre las 4 y 8 semanas de tratamiento, y a los 3 meses no tenían lesiones el 88,8%. El 87,5% no presentaban lesiones a los 6 meses. Los efectos adversos más frecuentes fueron el eritema y el prurito.
Conclusiones: a la vista de los resultados se puede considerar el tratamiento con Imiquimod al 5% como alternativa a otras terapéuticas destructivas, pudiendo tener a su vez, acción sobre la infección latente.
Palabras clave: Imiquimod. Condiloma. Eficacia. Efectos adversos
INTRODUCCION
Las verrugas genitales son una patología frecuente inducida por el virus del papiloma, que afecta con gran frecuencia a los jóvenes, que por lo general están producidas por los genotipos 6 y 111, que tienen manifestaciones clínicas e histológicas idénticas2. Se ha demostrado que cerca del 100 % de las verrugas genitales están causadas por los genotipos citados pero, que el 20-50 % de estas lesiones, también presentan co-infecciones por tipos de virus del papiloma humano de alto riesgo 3. Ocasionalmente, las verrugas genitales persisten durante periodos prolongados de tiempo, y en raras ocasiones estas lesiones duraderas pueden malignizarse. Una vez desarrolladas las verrugas genitales, pudieran presentar cambios mínimos a lo largo del tiempo, aumentar de tamańo, volverse más numerosas, o bien resolverse espontáneamente4. Las verrugas en regresión, contienen significativamente más células T CD4+, tanto en el estroma bajo las lesiones, como en la propia condilomatosis, y una mayor expresión de marcadores de activación5. Desde las épocas más antiguas, dadas las características de estas lesiones y que en muchas ocasiones son percibidas como antiestéticas y desfigurantes produciendo sensaciones vergonzantes a las pacientes, junto marcada ansiedad, se han tratado de establecer tratamientos6 que de la forma más sencilla y rápida se resolvieran las lesiones producidas por estos virus.
Pero el tratamiento de los condilomas no es sencillo, ya que las características de las lesiones, tamańo, condilomas múltiples y la localización en el aparato genital, son sin duda factores que dificultaban en ocasiones el instaurar tratamiento7, ya que en ocasiones, los tratamiento utilizados no se hacen de forma lógica y con frecuencia se observan tratamientos inadecuados apareciendo recurrencias, después de una aparente remisión8. Por estas causas, a lo largo de los ańos se han utilizado diversos tipos de tratamientos, desde la aplicación de variados tipos de pomadas, líquidos o de ungüentos, hasta la utilización de tratamientos más agresivos, como pueden ser la criocoagulación, la electrocoagulación, la vaporización con láser e incluso la resección con bisturí eléctrico9.
En los últimos tiempos, la utilización de Imiquimod en el tratamiento de los condilomas vulvo-perineales, se ha establecido como terapia de singular interés en este tipo de lesiones10. El Imiquimod actúa activando la secreción de citocinas y la inmunidad mediada por células que intervienen en la eliminación de las lesiones producidas por VPH.
El objetivo del presente estudio es conocer la respuesta del tratamiento de los condilomas vulvo-perineales, tratados con Imiquimod, y los efectos adversos derivados de su utilización.
MATERIAL Y MÉTODOS:
Diseńo de la investigación: estudio observacional prospectivo recogiéndose las pacientes para el estudio desde enero del 2005 hasta diciembre del 2009.
Población estudio: se han incluido 112 pacientes mujeres, con edades comprendidas entre los 18 y los 39 ańos, que fueron remitidas por presentar condilomatosis vulvo-perineal. Se excluyeron 7 con grandes masas de condilomas. Así mismo no se incluyeron pacientes gestantes, y las que eran VIH positivas se remitieron para otro estudio especifico. Todas las pacientes del estudio fueron sometidas a exploración ginecológica completa que incluía exploración clínica de genitales internos, junto con técnicas de imagen y exploración reglada del tracto genital inferior con: citología triple toma, recogida de muestra para genómica PCR mediante CLART HPV 2 y exploración colposcópica para cérvix y vagina después de pincelar con acido acético al 5% y posterior aplicación de lugol. Para la exploración vulvo-perineal, se utilizó el test de Collins (pincelación con azul de toluidina al 1% y posterior limpieza con acido acético al 1%). Se realizó exploración vulvoscópica en todas las pacientes, recogiéndose en el correspondiente protocolo, los siguientes parámetros: localización de los condilomas, tamańo de los mismos, así como número de ellos.
A las 112 pacientes seleccionadas, después de ser informadas sobre el tratamiento al que iban a ser sometidas, se les explicó la forma en la que tenían que realizar la aplicación del medicamento, en días alternos, por la noche al acostarse, aplicando una capa sobre todos los condilomas y realizando un lavado con agua y jabón al día siguiente por la mańana. El tiempo máximo de aplicación fueron 16 semanas. Se revisaron a las 4 semanas de iniciar el tratamiento, a las 8, 12 y 16 semanas.
Estudio estadístico: se realizó mediante el programa SPSS versión 17, implementado para PC. El IC fue del 95%.
Criterios de eficacia: viene establecida por el tamańo de la muestra estadística y el tiempo que estuvieron sometidas a tratamiento. Se realizó una detección de riesgos relativos de 1,75 o mayor y de 0,53 o menor. El tamańo de la muestra permitía un nivel de abandonos del 9%. El nivel de significación se estableció en 0,05.
RESULTADOS:
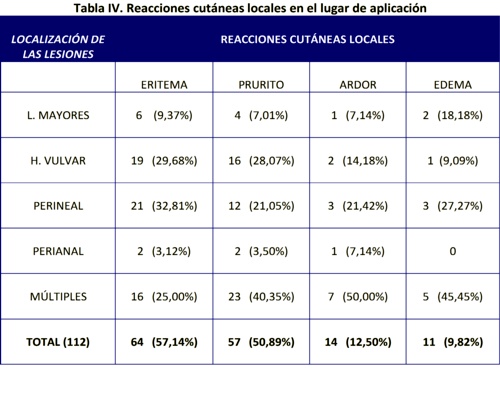
En la tabla I se describe la localización de las lesiones en las pacientes estudiadas. Predomina la localización de los condilomas en varias zonas, que identificamos como múltiples y alcanzan una frecuencia del 41,96% y que es significativa con relación a las otras localizaciones. Le siguen en frecuencia las que se encuentran solamente en la zona perineal con el 26,78%, y las de la horquilla vulvar, con el 20,53%.
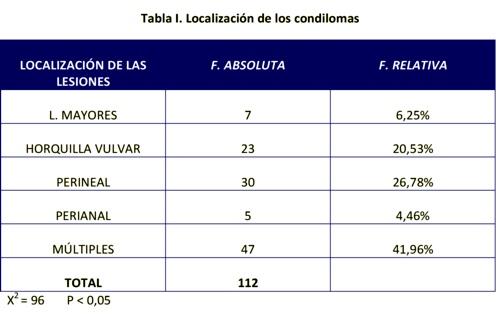
Tabla II. Se representa la respuesta al tratamiento a las 4, 8, 12 y 16 semanas. El mayor porcentaje de regresión se alcanza entre la cuarta y octava semana de tratamiento, predominando la desaparición de las lesiones de la horquilla vulvar, seguida de las localizaciones múltiples y los de la zona perineal, siendo significativos P<0,05, la respuesta del tratamiento con relación al resto de las lesiones tratadas. A partir de la 8Ş semana, en la 12 y en la 16, la disminución de las lesiones es menor, habiendo desaparecido todos los condilomas en la horquilla vulvar, persistiendo en mayor porcentaje los condilomas múltiples y los perianales, siendo el 87,5% las pacientes libre de lesiones en la semana 16.
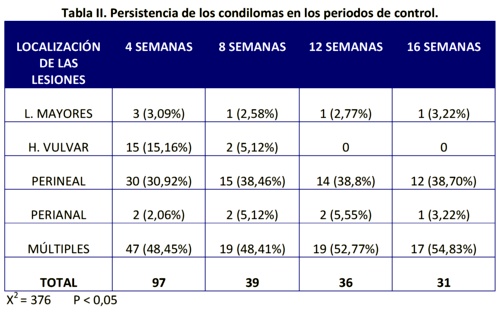
Tabla III. Se hace referencia a las recurrencias después del tratamiento. A los 3 meses no se habían reproducido en el 88,88%. El 7,40% de los condilomas en múltiples localizaciones habían vuelto a aparecer pero en muy escaso número, seguido de los de la zona perianal en el 2,46%. A los 6 meses persistían sin reaparecer el 87,5% de las pacientes tratadas
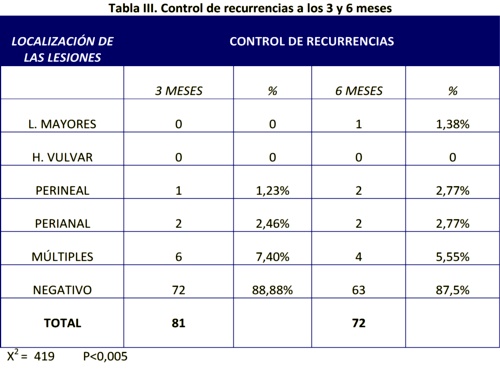
Tabla IV. Los efectos adversos detectados más frecuentes fueron el eritema en el 57,17% y el prurito en el 50,89%, siendo mucho menos frecuente el ardor, en el 12,5%, y el edema en la zona de aplicación, en el 9,82%.
DISCUSIÓN:
La eficacia del tratamiento de los condilomas es sin lugar a dudas la finalidad de todas las pautas que se han venido realizando11, aunque en realidad no existen muchos estudios que hagan referencia a los resultados, tanto de los tratamientos tópicos como de los destructivos. Por tratarse de lesiones benignas, hay autores12 que solo proponen el tratamiento por razones de higiene, riesgo de sobreinfección y en la mayoría de los casos por los factores psicológicos, ya que aumentan la ansiedad de las pacientes. En los casos de los condilomas vulvo- perineales producidos por el VPH, no podemos tratar la infección en sí misma, pero si las lesiones secundarias, aunque la curación clínica no significa una erradicación vírica, ni la pérdida de infectividad, debida a la persistencia de una infección latente posterapeútica en casi el 50 % de los casos13, lo que condiciona la aparición de recurrencias.
Los resultados de los tratamientos con imiquimod son muy variables. En un estudio con una población de 943 pacientes realizado por Aractingi14 se describe una respuesta global del 65,5% en la que se desglosa en mujeres el 75,5% y en hombres el 56,9%, siendo la tasa de recidivas a los 3 meses del 8,8% y a los seis del 23%. La reacción adversa local más frecuente fue el eritema, que se presentó en el 67% de los pacientes. Baya et al.15 realizaron un estudio comparativo en 50 pacientes tratadas con Imiquimod y 23 con técnicas destructivas, seńalando una incidencia de recidivas 6 veces menor en las tratadas con Imiquimod, siendo de un 7,6 % frente al 43,5% . La curación de las pacientes tratadas de forma tópica fue del 78%, siendo el 22% restante las que no completaron el tratamiento, bien por indicación médica, o por presentar efectos adversos marcados. Los autores detectaron la asociación de CIN y condilomas, en el 15% de las pacientes VIH negativas, y en el 71% de las VIH positivas, y la asociación de VIN en el 8,5% en VIH negativas y el 21,5% en las seropositivas.
Moore et al, en una revisión sistemática cuantitativa16, detectan en pacientes VIH negativas la remisión en el 51% de las pacientes tratadas con Imiquimod frente a un 6% tratadas con placebo. En tres ensayos, los resultados fueron más favorables para las mujeres, 72% de desaparición, frente al 37% en los hombres. Además, encuentra una reducción del área de la verruga al menos en el 50% en las pacientes tratadas, y las verrugas desaparecieron y no recurrieron en el 37%. Diamantis et al.17, tras una revisión de varios estudios, describen resultados similares en la eficacia del tratamiento con un rango que oscila entre el 50-71% de los pacientes con desaparición total de los condilomas. Los factores que determinan que no desaparezcan totalmente, o que la respuesta al tratamiento sea muy pequeńa, son la superficie de los condilomas, lógicamente a mayor superficie más dificultades para que haya una respuesta adecuada, y la queratinización, pues a mayor grado de ésta, la respuesta es menor. Otros de los elementos que hay que tener en cuenta con relación a la eficacia, es que la respuesta al tratamiento se realiza entre las 4 y 8 semanas, comenzando a reducirse la superficie de forma considerable; si no se realiza en esta época la reducción del condiloma, el tratamiento será ineficaz, circunstancia que hemos observado en el grupo estudiado por nosotros y que también ha sido referido por otros grupos de trabajo18,19. A pesar de todos estos parámetros, hay que tener en cuenta que como los tratamientos son realizados por la propia paciente, pueden existir circunstancias, como la forma y dificultad de aplicación según la localización de las verrugas, cantidad de producto utilizada y el miedo de la respuesta adversa, que pudieran modificar los resultados.
Los efectos adversos deben ser valorados, para completar la satisfacción ante el tratamiento. En la mayoría de los estudios, se valoraron las reacciones cutáneas locales en el lugar de aplicación, aunque no se informa de manera uniforme. Los efectos adversos más comúnmente referidos son, el eritema, el prurito localizado en la zona de aplicación, ardor y la erosión o escoriación. La intensidad de estas manifestaciones suelen estar presentes en intensidad leve y/o moderada, predominando el eritema y el purito, presentando porcentajes que están próximos al 60%, mientras que en los casos de efectos adversos severos, estos, han condicionado el abandono del tratamiento20. Ocasionalmente, se han descrito otros efectos como la vasodilatación cutánea y angioedema21 y la aparición de un ezcema severo22.
Las recurrencias después del tratamiento con Imiquimod al 5% se reducen de forma considerable, siendo estas bajas o poco frecuentes, aunque hay que reconocer que existe una marcada dispersión de datos que oscilan entre el 9 % y el 22%23,24 refiriendo Diamantis et al.17 una recurrencia del 19% a los 3 meses, y del 23% a los 6 meses. Las posibilidades de recurrencias vienen determinadas, por la carga viral, ya que a mayor carga, mayor posibilidad de recurrencia, poniéndose de manifiesto una clara disminución, en las pacientes tratadas con Imiquimod25. Este hecho es debido a la actividad antiviral indirecta del Imiquimod26. En los casos en que no exista desaparición completa de las verrugas, las residuales pueden ser extirpadas quirúrgicamente. En un seguimiento a largo plazo de 2-7 ańos, mostraron una tasa mucho menor de recidivas las pacientes tratadas con imiquimod más cirugía que las pacientes que fueron tratadas solo con cirugía27.
Así mismo, se ha valorado la respuesta al tratamiento con Imiquimod en las neoplasias intraepiteliales de vulva, pene y ano, asociadas a condilomas, o bien como patología aislada en la vulva. Las respuestas medias completas fueron del 51% en las neoplasias intraepiteliales de alto grado, mientras que en el 25% no se apreciaron remisiones completas de las lesiones y volvieron a aparecer después del tratamiento en el 16%. Aunque los resultados son prometedores, no existen estudios comparativos para valorar su eficacia contra las formas tradicionales de tratamiento28.
En resumen, teniendo en cuenta las características del virus del papiloma humano, epidemiologia, biología molecular, trasmisión de los virus, los factores psicológicos de las pacientes portadoras de condilomas por una parte, y los aspectos farmacológicos del Imiquimod, se puede considerar a este último un tratamiento alternativo a las pautas destructivas, pudiendo tener a su vez una acción sobre la infección latente.
Declaración de potenciales conflictos de interés: Todos los autores declaran no tener ningún conflicto de interés.
REFERENCIAS
-
1.-de Villers EM, Fauquet C,Broker TR,Bernard HU, Zur HH. Clasification of papillomaviruses Virology 2004;324:17-27.
2.- Gross G,Ikerberg H,Gissmann L, Gissmann L, Hagedorm M. Papillomavirus infeccion of the anogenital region: Correlation between histology, clinical oicture, and virus tipe. Proposal of a new nomenclature. J Invest Dermatol 1985;85:147-152.
3.-Lacey CJ. Therapy for genital human papillomavirus-related disease. J Clin Virol 2005;32:S82-90.
4.-Dunne EF, Unger ER, Sternberg M,Mcquillan G, Swan Dc, Patel SS et al. Prevalence of HPV infection among females in the United States.JAMA 2007;297:813-819.
5.- Lee PK, Wilkinns KB. Condyloma and other infections including human immunodeficiency virus. Surg Clin North Am 2010;90:99-112.
6.- Mahony C. Genital wart: Current and future management options. Am J Clin Dermatol 2005;6:239-243.
7.-Scheurer ME, Tortolero-Luna G, Adler.Storthz K. Human papillomavirus Infection: Biology, epidemiology and prevention. Int J Gynecol Cancer 2005;15:727-746.
8.- Heber CM, Laimimins LA. Human papillomaviruses basic mechanisms of pathogenesis and oncogenicity. Rev Med Virol 2006;16:83-97.
9.-Monteiro EF, Lacey CJ,Merrick D. The interrelation of demographic and geospatial risk factor between four common sexually transmitted deseases. Sex Transm Infect 2005;81:41-46.
10.-Mayeaux EJ, Dunton C. Modern management of external genital warts. J Low Genit Tract Dis 2008;12:185-192.
11.- Stefanaki C, Hadjivassilou M, Katzouranis I, Betimousltis G, Nicplaidou E, et al. Prognostic factors for the response to treatment in males with genital warts. J Eur Acad Dermatol Venereol. 2009;23:1156-1160.
12.- Renauud-Vilmer C. Infección de transmission sexual: Como tratar los condilomas de los genitales externos. Prac Ginecol Obst.2009; 44:4-5.
13.- Muńoz N, Kjaer SK, Sigurdsson K, Iversen OE, Hernandez-Avila M, Wheeler CM et al. Impact of human papillomavirus (HPV)-6/11/16/18 vaccine on all HPV-associated genital diseases in young women. J Natl Cancer Inst 2010;102:325-339.
14.- Aractingi S. Imiquimod en crema al 5% es un tratamiento seguro y eficaz para las verrugas genitales externas y perineales. 20 Th World Congress of Dermatology. Paris 1-5 Jul. 2002. Excerpta Méd. 2002: 12-13.
15.- Baya G, Centeno C, Xercavins J. Condiloma y su tratamiento. XI Cong. Of cervical Pathology and Colposcopy. Barcelona 9-13, Jun 2002. Excerpta Med 2002:6-7.
16.- Moore RA, Adwards JE, Hopwood J, Hicks D. Imiquimod for treatment of genital warts: A quantitative systematic review. Ach Dermatol 2002;138: 1599-1601.
17.-Diamantis ML, Bartiett BL, Tyring SK; Safety, Efficacy and recurrence rates of imiquimod Cream 5% for treatment of anogenital Warts. Skin Therapy Letter 2009;14: 1-3.
18.- Takahashi S, Tsukamoto T. Condyloma acuminatum. Nippon Rinsho 2009;67;153-156.
19.- Wagstaff AJ, Perry CM. Topical imiquimod: A review of its use in the management of anogenital warts, actinic keratoses, basal cell carcinoma and other skin lesions. Drugs 2007;67:2187-2210.
20.-Gunter J. Genital and perianal warts: new treatment opportunities for human papillomavirus infection. Am J Obst Gynecol 2003;189:3-11.
21.-Jacobs AA, Snavely N, Markus J, Rosen T. Vasodilatory adverse events associated with topical imiquimod 5 percent cream. Dermatol Online J. 2008;15:14-16.
22.- Taylor CL, Masien M, Kapembwa M. A case of severe eczema following use of Imiquimod 5% cream. Sex Transm Infect 2006;82:227-228.
23.- Beutner KR, Tyning SK,Trofaller KF. Imiquimod a patient-aplied immune-response modifier for treatment of external genital warts. Antimicrobial Agent And Chemot. 1998;42:789-794.
24.-Brodell LA, Mercurio MG, Brodell RT. The diagnosis and treatment of human papillomavirus mediated genital lesions. Cutis 2007;79:5-10.
25.- Schofer H. Evaluation of imiquimod for the therapy of external genital and anal warts in comparison with destructive therapies. Br J Dermatol. 2007;157:52-55.
26.- Hober D, Ajram L, Chehadeh W, Lazrek, M et al: Mecanismes de l'activité antivirale indirecte de l'imiquimod. Ann Biol Clin 2005;63:155-163.
27.-Carrasco D, Vander Straten M, Tyning Sk. Treatment of anogenital warts with Imiquimod 5% cream followed by surgical excision of residual lesions. J Am Acad Dermatol 2002;47:212-216.
28.-Mahto M,Nathan M,O'Mahony C. More than a decade on:Review of the use of Imiquimod in anogenital intraepithelial neoplasia. Int J STD AIDS 2010;21:8-16.
Correspondencia:
Ángel García Iglesias
Departamento de Obstetricia, Ginecología y Pediatría.
Facultad de Medicina de Salamanca.
Mail: aiglesias @ usal.es
