Indice del volumen Volume index
Comité Editorial Editorial Board
Comité Científico Scientific Committee
- Inconciencia
- Disminución del estado de alerta
- Discurso disperso o lento
- Letargo
- Movimientos lentos
- Mirada perdida o apatía.
- Hipervigilancia
- Cansancio
- Inquietud
- Discurso rápido o alto volumen,
- Irritabilidad o combatividad
- Impaciencia
- Comportamiento inapropiado como cantar, reír, poca cooperación, euforia, ira, coprolalia
- Distractibilidad fácil
- Respuesta motora rápida
- Tangencialidad
- Pesadillas o perseveración del pensamiento
- Inicio agudo: ocurre de manera abrupta, usualmente en un lapso de horas o días
- Curso fluctuante: los síntomas tienden a incrementar o decrecer en severidad en un periodo de 24 horas, existe una lucidez a intervalos
- Inatención: dificultad para concentrarse, mantener una conversación o seguir indicaciones
- Pensamiento desordenado: característicamente presentan discurso incoherente, conversaciones irrelevantes con ideas poco claras y con flujo ilógico de las mismas
- Nivel de conciencia alterado: respuesta estímulos externos se encuentra reducida junto con el estado de alerta
- Déficit cognoscitivo: típicamente se trata de un déficit global que incluye desorientación, alteraciones en la memoria y en el lenguaje
- Alteraciones sensoperceptuales: ilusiones o alucinaciones que se encuentran presentes en alrededor del 30% de los pacientes
- Alteraciones psicomotoras: dentro de las que se incluye el delirium hiperactivo, hipoactivo y mixto
- Ciclo de sueńo vigilia alterado: por lo general se presenta somnolencia durante el día, insomnio en la noche, sueńo fragmentado o ciclo completamente invertido
- Alteraciones emocionales: se manifiesta por labilidad intermitente, miedo, paranoia, ansiedad, depresión, irritabilidad, apatía, ira o euforia.
- D: Drugs (Drogas)
- E: Eyes, ears, emotional (Deprivación sensorial)
- L: Low oxigen states (Infarto agudo de miocardio, accidente cerebrovascular, tromboembolismo pulmonar)
- I: infection (infección)
- R: Retention (retención urinaria o fecal)
- I: Ictal (periodo posictal)
- U: Uncrontrolled pain (dolor no controlado)
- M: Metabolic (metabólicas)
- S: Subdural, por hematoma subdural. También ayuda a recodar al ser el plural, que un episodio puede tener diversas causas.
- Limite el número de intervenciones que deben realizarse en la atención del paciente
- Provea adecuada iluminación natural y seńalización clara en la habitación, procure tener disponible a la vista del paciente un reloj y un calendario
- Oriente al paciente frecuentemente, explicándole quien es y donde esta
- Realice actividades que lo estimulen cognoscitivamente
- Facilite la visita de familiares y amigos.
- Anime al paciente a beber agua, considere líquidos endovenosos en caso de que no sea posible beber
- Tenga en cuenta las patologías que pueden alterar al balance hídrico, tales como la falla renal, cardiaca entre otras y estabilícelas
- Valore la saturación de oxigeno del paciente y optimice el aporte del mismo en caso de ser necesario
- Evite cateterización innecesaria
- Utilice medidas de control de la transmisión de microorganismo
- Dolor:
- Evalúe signos verbales y no verbales de dolor
- Realice adecuado manejo
- Nutrición:
- Brinde adecuados suplementos y ajuste la dieta a la cultura del paciente
- Anime a la familia a estar presente en hora de alimentación
- Asegúrese que las prótesis dentales calcen perfectamente
- Asegúrese de que las ayudas visuales y auditivas están disponibles correctamente para el paciente, tales como lentes y audífonos según lo requiera.
- Promueva patrones normales de sueńo
- Evite procedimientos médicos y de enfermería durante la noche
- Evite horarios de medicación inapropiados
- Disminuya el ruido al mínimo en periodos de sueńo
- Evite las siestas durante el día.
- Amnesia Global Transitoria: asociada a convulsiones de cualquier tipo, produce profunda amnesia anterógrada y limitada retrograda, puede durar hasta 24 horas; evidencia alteraciones en la resonancia magnética nuclear principalmente luego de 48 horas.
- Amnesia Epiléptica Transitoria: Los episodios duran por lo general menos de una hora, son recurrentes y puede de manera inusual producir perdida de memorias autobiográficas remotas.
- Cambios en la memoria: żDebe utilizar más recordatorios de lo habitual? żTiene problemas siguiendo instrucciones?
- Cambios en el lenguaje: żLe es difícil encontrar palabras para hacerse entender?
- Cambios en la función viso espacial: żDificultades para la conducción, como conducir más lento para identificar peligros o aplicar los frenos tarde?
- Cambios en las funciones ejecutivas: żSe distrae con facilidad? żDificultades para la realización de las tareas del hogar?
- Es de gran utilidad recolectar información de los familiares o cuidadores a través de diferentes cuestionarios como el Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE) y el Dementia Severity Rating Scale (DSRS).
- Resonancia Magnética Nuclear: Se utiliza principalmente para predecir la posibilidad de progresión a demencia (acorde al volumen hipocampal36) y para descartar otras entidades, no se recomienda su uso de rutina.
- Exámenes de laboratorio: Están indicados para descartar patologías potencialmente reversibles.
DELIRIUM Y DETERIORO COGNOSCITIVO, I.
1Ángela María Benjumea Salgado MD, 2Sebastián López Velásquez MD, 2Laura María Cano Méndez MD.
1Medicina Interna y Geriatría y 2Cirugía, Universidad de Caldas.
Manizales, Caldas, Colombia.
Email: ambsco4 @ gmail.com
Rev Electron Biomed / Electron J Biomed 2018;2:39-61.
Comentario de la revisora Dra. Cynthia Marińansky . Geriatra de planta de la Unidad de Geriatria del Hospital Durand de Buenos Aires Directora de la Especialización en Geriatria Universidad Maimonides.
Comentario de la revisora Dra Silvina Dahl. Geriatra. Hogar Ledor Vador, Buenos Aires. Argentina.
RESUMEN
El envejecimiento es un tema que debe empezar a concentrar cada vez más la atención de los médicos y científicos en el mundo. Actualmente, en la mayoría de los países asistimos a dos eventos relacionados de suma importancia, la inversión de la pirámide poblacional, con una ampliación de la base de personas mayores y el incremento de la expectativa de vida. Si bien los trastornos cognoscitivos son altamente prevalentes en la población anciana, no son exclusivos de la misma y no debe asumirse, como solía hacerse, que éstos son una característica normal del trayecto de la vejez.
Este artículo expone una revisión completa y actualizada que aborda desde la fisiología hasta el enfoque diagnóstico y tratamiento de entidades claves como el delirium y el deterioro cognoscitivo, con énfasis en el mejoramiento de la calidad de vida de las personas afectadas e introduciendo conceptos destinados a orientar un envejecimiento exitoso.
PALABRAS CLAVE:
Deterioro cognoscitivo, delirium, Envejecimiento.
ABSTRACT
Aging is a subject that have increasingly concentrate the attention of physicians and scientists in the world. Currently, in most of the countries, we attend two important events, the transposition of the population pyramid, with an extension of the elderly population base and the increase in life expectancy. Although cognitive disorders are highly prevalent in the elderly population, they are not exclusive to them and it should not be assumed, as it used to be, that these is a normal characteristic of the path ageing.
This article presents a complete and updated review that addresses from physiology to the diagnostic approach and treatment of key entities such as delirium and cognitive impairment, with emphasis on improving the quality of life of the patients and introducing concepts in order to guide a successful aging.
KEY WORDS: Cognitive impairment, delirium, Aging.
INTRODUCCIÓN
El delirium y la demencia son causas comunes de deterioro cognoscitivo en el anciano; cada uno de ellos ocurre independientemente aunque con frecuencia coexisten. La demencia es el principal factor de riesgo para delirium y esto se refleja en el incremento de diagnóstico de nueva demencia y deterioro cognoscitivo después de diagnosticar un cuadro de delirium. Un episodio de delirium puede resultar con rápida progresión de síntomas de demencia con la consecuente discapacidad funcional, incremento en la carga del cuidador y costos de salud.
En la medida que la población envejece, se incrementa la incidencia y prevalencia de estas dos condiciones; es por ello que un mejor entendimiento de sus factores de riesgo, y las asociaciones entre ellos, es hoy en día una necesidad para desarrollar estrategias de prevención e intervención.
DELIRIUM
El delirium es una entidad común, típica aunque no exclusiva de la población anciana. Aparece con mucha frecuencia en los servicios de urgencias, hospitalización y también en las casas de atención a la vejez.
Lamentablemente, existe un imaginario colectivo en el personal de salud, tanto médico como de enfermería, que tiende a subestimar las implicaciones de esta patología, posiblemente debido a que no en todas las facultades se sensibiliza al estudiante de la salud a evitar el "viejismo" (prejuicio contra el anciano), lo que lleva a que en la práctica de su vida profesional incurra a menudo en éste, sesgándolo al momento de diagnosticar y tratar eficazmente las alteraciones del anciano.
Por otro lado, la relación estrecha del delirium y la demencia, se convierte en un factor contundente para la identificación acuciosa del primero, en nuestro medio esto es aún más relevante, pues gran parte del diagnóstico diferencial depende de la historia clínica y no es raro, sobre todo en las zonas rurales, que o bien no se dispone de un acompańante para realizar una adecuada anamnesis, o bien el nivel educativo bajo de éstos se convierte en una barrera para la determinación precisa de la información necesaria para hacer el diagnostico. Por último, y más importante, es preciso cambiar en el personal de salud, la concepción de que ya que el delirium se presenta con frecuencia y logra una resolución aparente a corto plazo, se trata de una entidad transitoria, sin consecuencias a futuro, dado que actualmente queda claro que cada episodio de delirium no solo contribuye a la declinación cognitiva del paciente anciano previamente diagnosticado con demencia o no, sino que también es claro que se encuentra ampliamente relacionado con un incremento importante en la mortalidad a corto y mediano plazo.
La presente revisión está diseńada pues, con el propósito de que los profesionales en formación en medicina general y especialistas, conciban la importancia de identificar y tratar el delirium, aportando herramientas prácticas para hacerlo.
Historia
El hecho de que el delirium se caracterice por síntomas polimórficos y volátiles al igual que por un curso fluctuante, junto con la falta plenamente identificable de un sustrato anatómico, ha llevado a que el concepto de delirium haya ido cambiando, desarrollado y comprendiendo de diferentes formas durante el curso de la historia y de una escuela a otra1.
Hipócrates, el padre de la medicina tradicional, describió por primera vez las condiciones de "Phrenitis" y "paraphrenitis" que hoy en día comprendemos como alteraciones comportamentales agudas observadas en la antigua Grecia, las cuales Hipócrates asoció con estados de inflamación.
El término delirium por su parte, ha sido utilizado por lo menos desde hace 2000 ańos, acuńado por primera vez por Aulus Cornelius Celsus en la antigua Roma, para describir desórdenes mentales. Allí se empleó también el término "Delirare", que del latín traduce algo así como "apartarse del surco", éste fue aplicado de manera general para aludir a alteraciones mentales sin referirse a una entidad especifica. De manera llamativa, Celsus también describió la "phrenitis" como un estado mental asociado a la inflamación, que oscilaba entre la euforia y la profunda tristeza, en medio de una aberrante locura desencadenada cuando alguien era apresado y reducido en la oscuridad.
Desde entonces hasta principios del siglo XIX, las condiciones de confusión mental fueron consideradas como un desorden psiquiátrico bastante estable que fue aprehendido por las diferentes escuelas europeas, describiéndose con múltiples variantes, pero conservando el mismo espíritu en común. Los alemanes por ejemplo, describieron muchos tipos de psicosis asociadas con alteraciones en la función cognitiva y cambios motores, relacionadas con varias enfermedades y con un nombre en particular para cada una de ellas, de esta manera empezaron a emplearse términos como manía aguda, psicosis exógena, locura sifilítica, entre otros.
Los franceses en cambio, fueron pioneros en adaptar una tendencia sindromática en la comprensión de los desórdenes psiquiátricos. Así pues, fue Peter Chaslin uno de los primeros exponentes de esta tendencia agrupadora, siendo también uno de los primeros en considerar que la actividad motora durante el delirium puede verse tanto incrementada como reducida.
El siglo XX fue la época de la controversia. El psiquiatra alemán Karl Bonhoeffer postuló que el cerebro puede reaccionar a irritantes exógenos de una forma inespecífica que depende de la constitución de la persona, lo que incluye la edad, los antecedentes, los metabolitos tóxicos a los que se haya visto expuesto, entre otros.
En ese entonces otras entidades relacionadas fueron descritas: la demencia, la amencia, estado crepuscular y Karl Jaspers fue el primero en describir como los síntomas de alteración de la conciencia se manifiestan durante las psicosis orgánicas.
El concepto moderno de delirium se le debe al psiquiatra Zbigniew J. Lipowski, quien lo postuló como una manera de denominar todo el espectro de perturbaciones de la conciencia vinculadas con alteraciones somáticas, junto con un estado incrementado, reducido o mixto de cambios en la actividad motora.
Epidemiología
El delirium es una de las enfermedades más frecuentes en los ancianos, su prevalencia al momento de admisión a unidades médicas reportada en estudios con adecuada realización, oscila entre el 10% y el 31% y la incidencia durante la hospitalización varía entre el 3% y el 29%2.
En general, los pacientes quirúrgicos son quienes presentan mayores tasas, especialmente en los posoperatorios de bypass coronarios, entre el 17% y el 74%; en cirugías ortopédicas va del 28% al 53% y es menor en cirugías urológicas, entre el 4.5% y el 6.8%.
Su prevalencia en las unidades de cuidado intensivo es alarmante, va del 60% al 80% en los pacientes con ventilación mecánica y del 20% al 50% en los pacientes sin ésta, y un nuevo campo de estudio que requiere más investigación comienza a figurar con altas tasas de presentación: las unidades de cuidado paliativo. Antiguas tendencias promovían que el delirium se debía a los agentes anestésicos, lo que hacía de éste una entidad inevitable, sin embargo numerosos estudios que han incluido las diferentes rutas de administración de los agentes anestésicos, han demostrado que no hay asociación2.
Recientemente en lo referente a las unidades de cuidado post-agudo se han demostrado dos cosas muy importantes. Primero, que los pacientes son dados de alta de los hospitales con un delirium sin resolver, lo que hace que éste persista por un largo periodo, en este sentido un nuevo campo de investigación epidemiológica se ha empezado a dirigir hacia las casas de cuidado post-agudo y a los asilos, donde se estima que la prevalencia del delirium se encuentra alrededor del 14%, siendo preciso aclarar si se trata de nuevos episodios agudos o cuadros persistentes tras hospitalizaciones.
En la comunidad en general, la prevalencia se ha estimado entre el 1% y el 2% la cual por supuesto se incrementa con la edad, llegando a cifras tan altas como el 14% en los mayores de 85 ańos. La mortalidad en los pacientes hospitalizados con delirium va del 22% al 76%, tan alto como en los pacientes con infarto agudo de miocardio o sepsis3.
Se considera que no se diagnostica esta entidad en alrededor del 32% al 66% de los casos y que quienes lo padecen, no recuperan su función cerebral global a su línea de base. Las consecuencias del delirium van desde complicaciones durante la hospitalización, perdida de la función, incremento de la estancia hospitalaria, alteración cognitiva prolongada y mayor mortalidad4.
La fisiopatología del delirium no se ha podido dilucidar con certeza, por lo que existen múltiples propuestas de mecanismos neurofisiopatológicos, la mayoría de las cuales están relacionadas con desbalances en la síntesis, degradación y liberación de neurotransmisores, dentro de los cuales se ha hablado de la dopamina, la acetilcolina, la serotonina, el GABBA y la noradrenalina; siendo los dos primeros aquellos que se han vinculado de una manera más poderosa a la generación de la patología, dada la plausibilidad que representa el déficit de la actividad colinérgica en la producción de los síntomas. Sin embargo, se han propuesto también otras vías de generación tales como el desarrollo de un mecanismo hipoxico-isquémico, inflamatorio e incluso se ha aludido a la existencia de una predisposición genética.
Extensa evidencia apoya el rol de la deficiencia colinérgica, pues medicamentos anticolinérgicos pueden causar delirium en animales y humanos, además se ha detectado actividad anticolinérgica sérica incrementada en los pacientes con delirium. El exceso de dopamina y su rol en el delirium, posiblemente en relación con su influencia reguladora en la acetilcolina, se ha demostrado en la medida en la que medicamentos dopaminérgicos como la levodopa y el bupropion se han identificado como precipitantes del delirium, mientras que antagonistas dopa como los antipsicóticos, logran tratar efectivamente los síntomas del delirium.
Los estados inflamatorios que promueven la producción de interleuquinas 1, 2, 6 y factor de necrosis tumoral, podrían contribuir con el desarrollo del delirium al aumentar la permeabilidad de la barrera hematoencefálica, alterando la neurotransmisión dependiente del flujo sanguíneo. Esto aplica no solo para los estados inflamatorios agudos, sino también para los estados de estrés crónico, dentro de los cuales también podría intervenir el característico hipercortisolismo, que se sabe ya, produce efectos deletéreos en los receptores hipocampales de serotonina3.
Un reciente estudio holandés del ańo 2015, investigó los niveles séricos de aminoácidos, proporción de los mismo y niveles de ácido homovalínico como indicadores de estrés oxidativo y alteraciones en la neurotransmisión en pacientes con enfermedad aguda mayores de 65 ańos, con el propósito de analizar las diferencias de dichos parámetros bioquímicos entre los pacientes con y sin delirium. Los comparó realizando un análisis de varianza en modelos ajustados por edad, sexo y comorbilidades, enfocando su estudio en el papel que cumple la alteración de la neurotransmisión serotoninérgica y el estrés oxidativo en la fisiopatología del delirium, teniendo como indicador neurobioquímico el tetrahidrobiopterin (BH4), un cofactor enzimático esencial para la síntesis de dopamina y serotonina, que actúa también como cofactor de la óxido nítrico sintasa en la producción de óxido nítrico y de citrulina a partir de arginina.
Una deficiencia en este cofactor se ha relacionado con una menor producción de serotonina y con la formación de superóxido en lugar de óxido nítrico y citrulina. Para su medición indirecta se utilizó la relación fenilalanina/tirosina sérica, con una razón elevada se indicaba deficiencia de BH4. Se midieron también otros aminoácidos y los niveles de ácido homovalínico. Este último es un metabolito de la dopamina indicativo de su producción cerebral hasta en 30%. Finalmente se midieron los niveles de arginina y citrulina. Como resultado se encontró alteración de la neurotransmisión serotoninérgica estadísticamente significativa y estrés oxidativo mayor en los pacientes que presentaban delirium que en aquellos que no. Además, se encontró que los niveles de homovalina fueron similares en ambos grupos, lo que no es indicativo de alteración en la vía de transmisión dopaminérgica5. A pesar de lo que parecen ser resultados impactantes en la dilucidación de la fisiopatología del delirium, estos no son generalizables por las mismas debilidades que los autores reconocen en su realización, sin embargo, dichos resultados abren una perspectiva de investigación diferente a las tendencias que se venían manejando en el descubrimiento de la fisiopatología de una enfermedad. Por otra parte, desde el punto de vista anatómico, estudios electroencefalográficos han demostrado en los pacientes con delirium, disminución difusa de la actividad cortical que no se correlaciona con las causas subyacentes. Estudios neurofisiológicos y de neuroimagenológicos han evidenciado disrupción generalizada en la función cortical más alta como en la corteza frontal anterior y de igual forma en estructuras subcorticales como el tálamo y los ganglios basales, seńalando especialmente alteraciones en la corteza innominada. Sin embargo, en términos de eficiencia diagnostica, el electroencefalograma tiene una tasa de falsos negativos del 17% y falsos positivos del 22%, de igual manera las neuroimágenes tienen un valor limitado y deben reservarse para los casos de focalización neurológica de inicio agudo.
Características clínicas
Aunque un solo factor puede desencadenar el delirium, se ha descrito un modelo multifactorial en el desarrollo del mismo que ha sido ampliamente validado y aceptado. Así pues, se sabe que depende de una compleja interrelación entre pacientes vulnerables con varios factores predisponentes y la exposición a noxas o factores precipitantes. El conocimiento de este comportamiento permite entonces diseńar estrategias más efectivas en la prevención del delirium, dado que muchos factores de riesgo para delirium han sido identificados y los factores precipitantes se sabe que varían de acuerdo con el tipo de población, de manera tal que estos interactúan en una relación inversamente proporcional, lo que significa que en un paciente con muchos predisponentes se necesitan escasos precipitantes para desencadenar la enfermedad y en uno con pocos predisponentes se ha de requerir mayor número de precipitantes. A continuación se resumen dichos factores (Tabla 1):
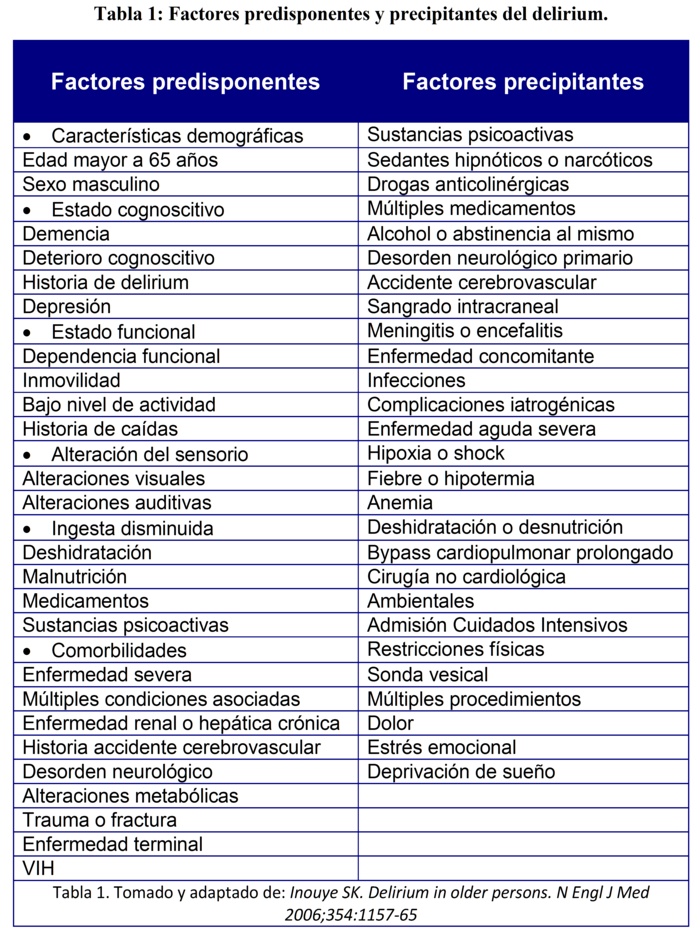
Por otro lado en lo que tiene que ver con la identificación de la patología al momento de presentarse, debe tenerse en cuenta que desde el punto de vista psicomotor se reconocen 3 subtipos de delirium6:
-
a) hipoactivo,
b) hiperactivo y
c) uno mixto.
Los ancianos por lo común presentan la forma hipoactiva, que generalmente pasa desapercibida y consiste en al menos 4 de los siguientes:
Por otro lado el delirium hiperactivo se diagnostica con 3 de las siguientes características:
El mixto es el que se diagnostica más frecuentemente
Aproximación diagnostica
Al momento de hacer el diagnostico, se deben tener claro que la semiología del delirium se compone de los siguientes aspectos:
Estas características han sido dividas en aspectos clave y de apoyo para mejorar la certeza del diagnóstico, los aspectos claves constituyen la agudeza del episodio, el curso fluctuante, la inatención, alteración de la conciencia y cognitiva. Se conciben como características que apoyan el diagnostico la alteración del ciclo sueńo vigilia, las alteraciones perceptuales y psicomotoras, el comportamiento inapropiado y las alteraciones emocionales. Determinar que la confusión es un episodio agudo o no, es el primer paso para no fallar en el diagnóstico del delirium, si la historia clínica no puede ser obtenida completa, deberá sospecharse hasta demostrar lo contrario.
Herramientas diagnosticas
Aunque los criterios diagnósticos estándar se encuentran consignados en el DSM5 y el CIE 10, existen más de 24 instrumentos que han sido usados para el diagnóstico del delirium. Los criterios CAM (confussion Assessment method), que se especificaran más adelante, son los más ampliamente utilizados y validados, han sido usados en al menos 4000 estudios publicados y traducidos a al menos doce idiomas. Su aplicación se recomienda en combinación con un test cognoscitivo corto, como por ejemplo el Minimental test. Tenga en cuenta que dichos criterios han sido adaptados para ser aplicados en las unidades de cuidado intensivo y en el servicio de urgencias. Revise las lecturas recomendadas para conocer cómo se modifican en dichos escenarios7-9.
Existen también herramientas diagnosticas en la estimación de la severidad del delirium, dentro de ellas encontramos el delirium Rating Scale, y el Memorial delirium Assesment Scale, las cuales constituyen las escalas con mejor evidencia clínica para tal fin10.
Otra opción que puede utilizar para realizar el diagnostico, son los criterios Family Cam o FAM-CAM, con el cual es posible hacer el diagnostico en torno a las referencias orales informales brindadas por los familiares y los cuidadores del paciente.
Criterios CAM:
-
1. Inicio agudo y curso fluctuante
2. Inatención
3. Pensamiento desorganizado
4. Nivel de conciencia alterado
El diagnostico se hace con la presencia de los criterios 1 y 2 junto con cualquiera de 3 o 4
Manejo del delirium
Existen tres pilares del manejo del paciente: garantizar la seguridad del paciente, proveer tratamiento adecuado a las causas y manejar los síntomas11.
En términos de seguridad, los esfuerzos deben dirigirse a proteger la vía aérea y prevenir la aspiración, mantener una adecuada nutrición e hidratación, prevenir escarificación de la piel y proveer una movilidad segura previniendo caídas, sin olvidar realizar tromboprofilaxis y brindar atención oportuna a las necesidades fisiológicas de los pacientes. Las restricciones físicas no son recomendadas, ni en pacientes en riesgo, ni en los que ya han desarrollado delirium, pues se asocian mayor severidad del mismo y con lesiones físicas.
La segunda acción que debe realizarse es identificar las causas del delirium y tratarlas efectivamente. En cuanto a la determinación las causas subyacentes del delirium, se debe tener en cuenta que éste muchas veces hace parte de una manifestación atípica de entidades que amenazan la vida, tales como infarto agudo al miocardio, infecciones y falla respiratoria. No se debe olvidar que tanto los medicamentos instaurados recientemente como los de larga data pueden contribuir a la presentación de esta entidad, y para que esta búsqueda de causas sea exhaustiva, se recomienda seguir la mnemotecnia deliriumS, un fácil acrónimo en inglés que puede ayudar a sospecharlas e identificarlas minuciosamente:
En cuanto a la asociación causal con drogas, tenga en cuenta la siguiente tabla para identificar el riesgo que representa la medicación actual que tiene el paciente (Tabla 2):
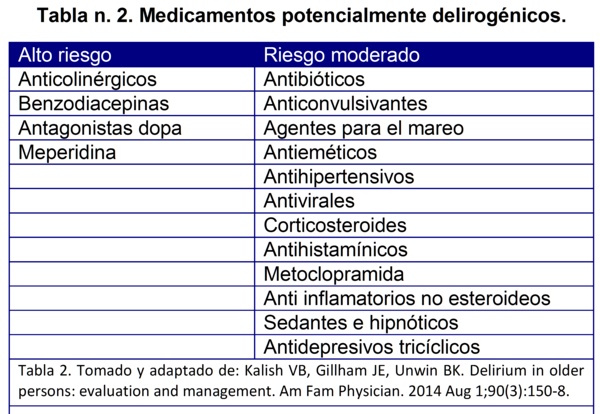
En el manejo de los síntomas las recomendaciones giran en torno tanto a las intervenciones farmacológicas como a las no farmacológicas, teniendo en mente que las no farmacológicas incluyen tanto la descontinuación o reducción de la dosis de medicamentos con efecto anticolinérgico y drogas psicoactivas, implementar el acompańamiento de la familia para proveer reorientación y confort y para la creación de un ambiente silencioso y cálido, puesto que sacar al anciano de su ambiente y colocarlo en un escenario hospitalario constituye per se, un fuerte desencadenante del delirium que debe ser atenuado al máximo.
Prevención y medidas no farmacológicas
Las medidas no farmacologías, podremos agruparlas de la siguiente manera, dependiendo del sistema afectado:
Alteraciones cognoscitivas o desorientación:
Hidratación/constipación:
Hipoxia:
Infecciones:
Alteraciones del sensorio:
Sueńo:
Medidas farmacológicas
Estas deberían reservarse para aquellos pacientes severamente agitados que ponen en peligro su propia seguridad o la de los demás. Aunque los antipsicóticos se han asociado como desencadenantes en algunos pacientes, el haloperidol es el que tiene mejor evidencia y es más ampliamente utilizado, a pesar de sus efectos extrapiramidales. Estos medicamentos deben emplearse previa valoración adecuada del paciente y como último recurso sin aplicarse indiscriminadamente, la olanzapina disminuye la incidencia pero incrementa la severidad y duración del delirium. La siguiente tabla puede ofrecerle una guía para el uso de los antipsicóticos en delirium (Tabla 3)
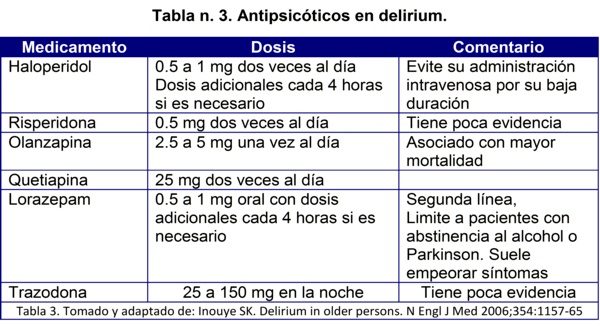
Los últimos intentos farmacológicos en incrementar el aporte de acetilcolina con agentes como rivastigmina, o antagonistas de la dopamina con acción en los receptores d1, d2, d3, d4, han terminado en incremento de la mortalidad. Otros esfuerzos por incrementar el flujo sanguíneo por medio de por ejemplo, antiinflamatorios o antiplaquetarios, no cuenta aún con suficiente evidencia.
Delirium y demencia
Se encuentran íntimamente relacionados, pero la naturaleza de su interrelación no ha podido ser dilucidada, sin embardo, la dificultad para la diferenciación entre estos dos diagnósticos, se cree es una de las razones más importantes por las cuales el delirium pasa desapercibido.
El nivel de conciencia alterado es una excelente clave para diferenciarlos cuando no es posible conocer el estado de base del paciente. Tenga en cuenta que la orientación depende de la memoria y se encuentra frecuentemente alterado en ambos desordenes. El diferenciador clásico es entonces el inicio agudo y el curso fluctuante de los síntomas en el delirium. La tabla 4 puede ser útil en el diagnóstico diferencial:
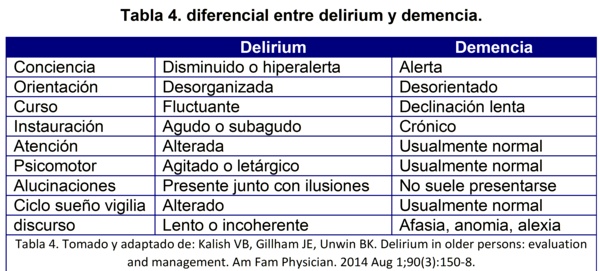
El hecho de que el delirium sea simplemente un marcador de vulnerabilidad a la demencia o de si este por sí mismo tiene la capacidad de llevar a la demencia, es un punto de mucha controversia, pero recientemente se ha identificado que ambas hipótesis pueden ser reales. Un episodio de delirium marca una seńal de la vulnerabilidad de un cerebro con reserva cognoscitiva disminuida e incrementa el riesgo de demencia a futuro.
Estos dos frecuentemente coexisten y la demencia es un factor de riesgo para el delirium, sin embargo ya existe una gruesa evidencia epidemiológica de como el delirium lleva al desarrollo de demencia e induce una declinación cognitiva en los pacientes que ya la tienen.
Datos recientes sugieren que el delirium tiene una duración mayor a la que se creía previamente, con síntomas en muchos pacientes que duran meses y hasta ańos, lo que borraría los límites entre el delirium y la demencia. Fisiopatológicamente, la relación de estos dos se encuentra en la disminución del metabolismo cerebral, la deficiencia colinérgica y la inflamación, reflejando la sobreposición entre sus mecanismos clínicos, metabólicos y celulares, de hecho, se especula que sean en realidad un espectro continuo más que dos entidades separadas.
El delirium como marcador de la calidad de la atención: el delirium representa un marcador de calidad de la atención en salud porque es altamente prevenible, se ha calculado que lo es en el 30 al 40% de los casos y cumple con los criterios de Williamson para ser indicador de la calidad de la atención en salud: es una condición común, frecuentemente iatrogénica e integralmente vinculada a proceso de cuidado3.
MEMORIA
Las funciones cognoscitivas son aquellas que nos llevan al aprendizaje y por ende al conocimiento, como una característica de los seres humanos. Las más estudiadas son la memoria, el lenguaje, el juicio, el raciocinio, la abstracción, la secuenciación y el pensamiento. Todas ellas se relacionan entre si y dan como resultado, la capacidad del ser humano de interactuar con los demás y a su vez, de entender, transmitir y crear. El conocimiento es en esencia el producto de su combinación y su principal aliada, es la memoria, siendo esta alteración la que mayor compromiso va a tener sobre el mismo12.
La memoria es considerada como una colección de habilidades mentales que dependen de la totalidad de la corteza cerebral (pero que tienen localizaciones especificas donde se da mayor cantidad de interconexiones), y que le permiten procesar la información que estará disponible posteriormente.
La clasificación de memoria de corto y largo plazo ya no se utiliza debido a que los múltiples estudios han permitido mejor comprensión de la misma y una clasificación mucho más acertada.
Se consideran cuatro tipos de memoria: episódica, semántica, procedimental y de trabajo; además de lo anterior algunos están asociados a la consciencia (explícita) y pueden ser recordadas a voluntad (declarativa), mientras que otras son expresadas a través del comportamiento (implícita) y por lo general se dan de manera inconsciente (no declarativa), existen otro tipo de clasificaciones acorde a la naturaleza de lo que se quiere recordar como visual o viso espacial (Tabla 5).
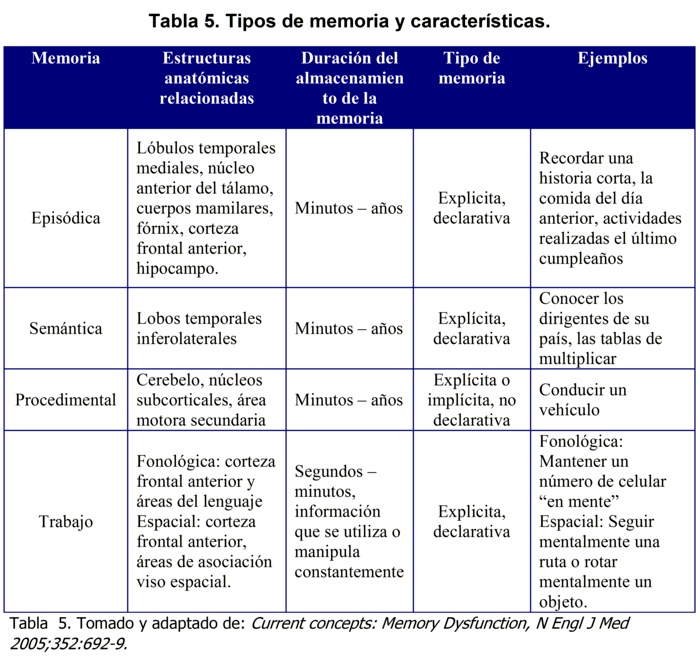
Memoria Episódica
Ha tenido múltiples definiciones a lo largo de su historia, sin embargo, consideramos que la siguiente aborda la mayoría de conceptos fundamentales que requiere para entender su funcionamiento. Se define entonces, como la capacidad consciente para recordar episodios y experiencias personales (el almuerzo de ayer, el nombre de la mamá, caída en bicicleta a los 6 ańos) que involucra una serie de pasos como codificación, consolidación y recuperación. Por lo tanto, es explícita y declarativa13. Esta definición incluye los dos componentes fundamentales de la memoria episódica: Concepción de sí mismo y del tiempo, responde a las preguntas: żQué? żCómo? żCuando?
La codificación hace referencia a la dirección de los procesos cerebrales mediados principalmente por el componente atencional, la consolidación involucra el almacenamiento de la información de manera que sea accesible en el futuro y la recuperación es el acto de recordar la información.
Su existencia fue clínicamente diferenciada de otras funciones cognitivas en 1957 cuando Milner y Scoville14 reportaron el caso de Henry Molaison (conocido en la historia de la medicina como paciente H. M.) quien vivió de 1926 a 2008, presentaba una epilepsia refractaria al tratamiento por lo que le realizaron resección bilateral de los lobos temporales mediales, posterior a lo cual demostró profunda amnesia anterógrada (incapacidad de formar nueva memoria episódica) verbal y no verbal, además presentó una amnesia retrograda (incapacidad para acceder a memoria episódica del pasado) en menor medida; sin alterar las otras funciones.
Neuroanatomía:
Si bien con el paciente H. M. se estableció la relación directa con el lobo temporal, estudios neuropsicológicos y neuropatológicos han demostrado que existe alteración hipocampales de gran importancia (principalmente en las subregiones CA1 a CA3, giro dentado y fórnix), extrahipocampales (corteza entorrinal, perirrinal y corteza parahipocampal), circuito de Papez (cuerpos mamilares, núcleo anterior del tálamo) y la corteza frontal13. Esta última tiene un papel fundamental como coordinador del proceso de codificación y recuperación, por lo que las alteraciones en la corteza frontal generan distorsiones como memorias falsas, información asociada con el contexto equivocado y detalles específicos incorrectos; para hacer un esquema de la relevancia de estos componentes, la corteza frontal es la encargada de distribuir los archivos, los lobos temporales y circuitos hipocampales "almacenan" los archivos recientes y las otras regiones corticales "almacenan" los archivos antiguos12. Es importante entender que en el cerebro humano no se almacena como tal la información, sino que se reconstruye a partir de las necesidades y circuitos neuronales.
Actualmente el estudio del hipocampo ha cobrado gran importancia en el estudio de la memoria llevando al concepto de estimulación episódica, en la cual se analiza que, si los recuerdos conducidos por el hipocampo son relacionales, reorganizarlos para reconstruir nuevos escenarios es también capacidad hipocampal15. Esta estimulación episódica hace parte importante en la emocionalidad de los recuerdos, siendo asociada en múltiples estudios no solo con mejor capacidad para consolidación y recuperación sino con mejor capacidad de resolución de problemas sociales, empatía y voluntad para ayudar personas en necesidad16-17 entrando entonces en el campo de la medicina evolutiva.
Alteraciones de la memoria episódica:
El abordaje que haremos acá será a partir de la temporalidad del compromiso:
Agudas: Traumatismos cerebrales, contusión, evento cerebrovascular que compromete la arteria cerebral posterior18. Generalmente tienen mejoría lenta.
Subagudas: Entidades infecciosas (encefalitis, meningitis), Síndromes para neoplásicos, causas tóxicas/metabólicas como el síndrome de Korsakoff.
Transitoria19:
Crónicas: Procesos neurodegenerativos (demencias), esclerosis hipocampal asociada al envejecimiento (asociada generalmente a alteraciones cerebrovasculares)20
Memoria Semántica
Al igual que la memoria episódica es explicita y declarativa, se trata del conocimiento adquirido por el individuo acerca del mundo, sus relaciones y usos, incluyendo hechos, conceptos, palabras y sus significados. Su contenido es abstracto, de la experiencia y generalización, no necesariamente con referencia a un episodio autobiográfico especifico13, 21.
Se trata de la llamada "cultura general", a la cual se le ha dado lastimosamente la connotación de información innecesaria en muchas ocasiones, pero es fundamental para todos los procesos incluyendo la medicina, por ejemplo: es fundamental conocer cómo se realiza una toracotomía ya que puede salvar la vida de pacientes con neumo o hemotórax, siendo igual de importante conocer la anatomía del tórax y la fisiología pulmonar. Por lo cual la "cultura general" constituye la base del conocimiento.
Las palabras que se usan con poca frecuencia como los nombres propios se alteran inicialmente, llevando a los pacientes a realizar sustituciones parafrásicas (dar nombres que no corresponden) o a mencionar categorías de orden superior (denominar como carros en lugar de mencionar automóvil, camión)13.
A diferencia de los cuadros de anomia pura, las alteraciones de la memoria semántica persisten aun cuando a los pacientes se les brinda el nombre en cuestión.
Es muy importante la detección de las alteraciones, vigilancia y manejo pertinente ya que las alteraciones más profundas (en las que típicamente se presenta el déficit de la nominación en doble sentido la cual consiste en la incapacidad de nominar un objeto descrito o de describir un objeto nominado) pueden llevar a una pérdida del conocimiento del objeto, lo cual pone en riesgo al paciente (colocar a cocinar objetos que no son comida). Debe sospecharse alteraciones en personas con dificultades en la nominación de objetos que antes conocía.
Neuroanatomía
Al igual que en todos los tipos de memoria ubicar la memoria semántica es difícil debido a la enorme cantidad de interacciones que tiene, ya que incluye información del sistema límbico, los sentidos, la interpretación personal, entre otros; sin embargo, se ha encontrado que pacientes con alteraciones semánticas puras, presentan alteraciones de predominio (no exclusivo) temporal inferolateral y anterior12.
En los pacientes con afasia progresiva primaria se ha estudiado a través de neuroimágenes, la ubicación neuroanatómica de la lesión encontrando que el lobo temporal anterior funciona como centro amodal (inespecífica motora o sensitiva), que funciona como enlace entre las diferentes modalidades21.
Este tipo de memoria presenta lateralización, se ha evidenciado que pacientes con alteración en el giro fusiforme izquierdo presentan mayores alteraciones verbales (nombre de los colores) y las alteraciones en el giro fusiforme derecho alteraciones no verbales (reconocimiento de carros, casas, lapiceros)22.
Alteraciones de la memoria semántica:
La enfermedad por excelencia para las alteraciones en la memoria semántica es la afasia progresiva primaria caracterizada por anomia, que precede la pérdida del conocimiento por los objetos, los trastornos de la expresión del pensamiento pueden llevar incluso al mutismo, también se evidencian alteraciones comportamentales dentro del curso de la enfermedad.
Igualmente se produce alteración en la enfermedad de Alzheimer, sin embargo, las características de declinación no son tan pronunciadas; curiosamente las categorías semánticas más comprometidas en la afasia progresiva primaria y la enfermedad de Alzheimer difieren si se solicita la identificación de objetos naturales o sintéticos23,24.
Memoria de Trabajo
Consiste en el mantenimiento de la información verbal o no verbal en la "mente" para potencial manipulación con el fin de completar una tarea determinada, es dependiente de la atención y concentración, por lo general una vez se cumple el propósito es olvidada (no se da así en personas con hipermnesia o también llamada memoria eidética),este tipo de memoria generalmente ha sido asociada a las funciones ejecutivas debido a sus características, al igual que los tipos de memoria anteriores se trata de una explicita y declarativa12,13.
Tiene dos componentes: el primero fonológico como la capacidad de mantener un número de celular en la "mente" y el segundo espacial como la capacidad de seguir mentalmente la ruta hasta la casa. Se han propuesto otras divisiones con la que considera también dos tipos de memoria episódica: de tareas que requieren únicamente mantener información (repetir una serie de números) y la de tareas que requieren manipulación activa de la información (describir la misma serie de números, pero en sentido contrario u organizarlos de mayor a menor)12.
Este tipo de memoria es fundamental para actividades de alto nivel como planeación, toma de decisiones ya que nos permite mantener al tanto de toda la información necesaria.
Neuroanatomía:
Debido a sus características la memoria de trabajo requiere la corteza frontal anterior, al igual que interconexiones a nivel cortical y subcortical, comprende las áreas de asociación tanto motoras como visuales, la información fonológica y espacial demuestran mayor actividad cortical en el hemisferio izquierdo y derecho respectivamente (recordar que no existe a nivel cerebral procesos que ocurran en un hemisferio particularmente y que las interconexiones comprenden toda la masa encefálica por lo general)12.
Alteraciones de la memoria de trabajo:
Debido a la extensión de circuitos que involucra, la gran mayoría de enfermedades neurodegenerativas la comprometen como: enfermedad de Alzheimer, Huntington, Parkinson, demencia por cuerpos de Lewy y parálisis supranuclear progresiva; Igualmente las accidentes cerebro vasculares, trauma en cabeza, tumores y debido a la dependencia de la atención que tiene la memoria de trabajo, las enfermedades con el déficit de atención e hiperactividad, trastorno obsesivo compulsivo, esquizofrenia y depresión también pueden alterarla25.
Memoria Procedimental
Se trata de la capacidad de adquirir (con práctica) habilidades cognoscitivas, comportamentales y procedimentales que posteriormente operan de manera automática13,26.
Este tipo de memoria es no declarativa e implícita, sin embargo durante la adquisición del conocimiento es explicita ya que requiere atención, consolidación de los diferentes pasos y luego ponerlo en práctica, un ejemplo muy claro es cuando se está aprendiendo a conducir un vehículo; se requiere conocer el uso y localización de los pedales, al igual que la palanca y el manubrio, aunado a lo anterior debe tenerse en cuenta las seńales de tránsito, las condiciones de la vía y los otros vehículos; al inicio a todos nos cuesta tiempo, pero luego ya incluso se pueden sostener conversaciones mientras se realiza.
La memoria procedimental es fundamental para nuestra especie, nos permitió (y permite) reproducir las actividades y actitudes de los mayores lo que nos generó capacidad de adaptación, supervivencia y reproducción26.
Neuroanatomía:
Es de esperar por sus características que la localización neuroanatómica esté en estrecha relación con las estructuras motoras, se ha encontrado a través de neuroimágenes, en pacientes con alteración de este tipo de memoria, lesiones principalmente en el área motora secundaria, cerebelo y los núcleos subcorticales (mal llamados ganglios basales)12.
Alteraciones de la memoria procedimental:
La enfermedad que produce mayores alteraciones en este tipo de memoria es la enfermedad de Parkinson27, que generalmente no responde al tratamiento estándar; otras enfermedades incluyen enfermedad de Huntington y enfermedades ponto degenerativas. Al igual que los tipos de memoria anteriores los tumores, accidentes cerebro vasculares, hemorragias, depresión y traumas la pueden alterar.
DETERIORO COGNOSCITVO LEVE
Se trata de un estadio clínico en el continuo de la declinación cognoscitiva, que se encuentra entre lo que es considerado normal por el proceso de envejecimiento y la demencia28,29.
Se caracteriza por alteración cognitiva que no es lo suficientemente severa para requerir ayuda en las actividades de las vidas diarias básicas, instrumentales o avanzadas. Con esta definición queda clara la principal diferencia con la demencia: preservación de la independencia en sus actividades de la vida diaria, incluyendo una participación activa en el entramado social.
Los criterios diagnósticos de la The National Institute on Aging-Alzheimer´s Association (NIA-AA) en el 2011 para el Deterioro Cognoscitivo Leve (DCL) son30:
1. Preocupación del paciente por un cambio en su capacidad cognoscitiva, evidenciable por un informante o por el personal del equipo de salud
2. Evidencia objetiva del deterioro (mediante las diferentes pruebas) en uno o más dominios cognoscitivos, incluyendo memoria, función ejecutiva, atención, lenguaje y habilidades viso-espaciales.
3. Preservación de la independencia en las Actividades de la vida diaria básicas, instrumentales y avanzadas (se debe tener en la cuenta que los pacientes pueden ser menos eficientes y cometer errores en estas actividades)
4. Sin evidencia de compromiso social u ocupacional (no se encuentra en una demencia)
También existe una entidad conocida como deterioro cognoscitivo leve debido a enfermedad de Alzheimer definida como: "Aquellos pacientes sintomáticos, pero no dementes, cuya fisiopatología primaria es una enfermedad de Alzheimer", se caracteriza por un deterioro en la memoria, declinación longitudinal en la función cognoscitiva, sin evidencia de otras causas de deterioro cognoscitivo (vascular, traumático u otras condiciones).
De acuerdo con las alteraciones se ha dividido en: amnésico, no amnésico (disejecutivo) y multidominio.
El DCL tipo amnésico es el más común (65%) teniendo una relación con el tipo no amnésico de 2:1, en este tipo se compromete únicamente la memoria episódica, respetando los otros tipos de memoria, los pacientes que progresan a demencia lo hacen generalmente a demencia tipo Alzheimer28.
Por su parte, el tipo disejecutivo se asocia con compromiso de alguna función diferente a la memoria y en su gran mayoría se relaciona con alteraciones en la ejecución, planeación, secuenciación, entre otras. Corresponde aproximadamente al 25% de los pacientes y cuando progresan a demencia, generalmente lo hacen hacia tipos frontotemporales o subcorticales.
El tercer tipo es el multidominio (alrededor del 10% de los pacientes). Se caracteriza por tener al menos 2 funciones cognoscitivas comprometidas (en menos de una desviación estándar). La gran mayoría cuando progresan a demencia lo hacen hacia la tipo Alzheimer.
Epidemiología y Factores de Riesgo
La prevalencia de DCL en los mayores de 60 ańos es del 6.7% al 25.2%. Aumenta con la edad y el bajo nivel educativo y es más prevalente en los hombres28. La progresión anual a demencia es del 5% al 17% aproximadamente29. Algunos biomarcadores asociados a la progresión a enfermedad de alzheimer son la presencia de la apolipoproteina E4, niveles de proteína tau alterados en liquido cerebroespinal y una PET positiva dado por depósitos de tau en las estructuras laterales del lóbulo temporal29,31.
El 54% de los pacientes presentaban DCL tipo amnésico y estos pacientes fueron los que más portaban la APOe4, además el 81% de los pacientes que progresaron a demencia provenían de este tipo de DCL.
Valoración de un paciente con Deterioro Cognoscitivo Leve
Es importante que a todos los pacientes con sospecha de DCL se les realice una completa y correcta historia clínica, además de un minucioso examen físico, enfocándose principalmente en la función cognoscitiva, capacidad funcional, medicamentos, patologías neurológicas o psiquiátricas y exámenes de laboratorio. El objetivo primordial consiste en diferenciar un DCL de una demencia además de identificar causas reversibles (depresión, reacciones de los medicamentos, patología tiroidea, déficit de vitamina B12 o de folatos, entre otras)32,33.
Para evaluar la función cognitiva en el transcurso del tiempo es fundamental entablar una buena relación médico-paciente-familiares, ya que los síntomas pueden ser infravalorados por el paciente y sobrevalorados por los familiares o cuidadores, principalmente con el fin de evitar discusiones. Se recomienda realizar las siguientes preguntas:
Además de lo anterior, se deben aplicar los diversos instrumentos para evaluar la capacidad cognoscitiva, dentro de estos el más recomendado es el MoCA (The Montreal Cognitive Assessment), con punto de corte de 24/25 puntos. La sensibilidad y especificidad de la prueba es de 80.48% y 81.19%, respectivamente34.
El Minimental test no se recomienda como instrumento de tamización debido a que diversos factores como la cultura, educación y el lenguaje. Por ejemplo, el nivel educativo afecta el Minimental en los dominios no asociados a memoria como la orientación, atención y lenguaje35.
Una comparación directa entre el minimental y el Moca, reportó que este último es más sensible para diferenciar personas con DCL de a aquellos con función cognoscitiva normal32.
En cuanto a la capacidad funcional múltiples estudios indican la aplicación del cuestionario The Functional Activities Questionnaire (FAQ), encontrando que un punto de corte de 6 o mayor tiene una tasa de exactitud del 85% para diferenciar pacientes con DCL de los que presentan demencia32,33. Sin embargo consideramos que la valoración de las actividades de la vida diaria con las escalas de Barthel, Lawton modificada y la escala de Lawton y Brody, nos brindan mucha más información para dilucidar la situación del paciente.
La revisión de los medicamentos es fundamental ya que existen diferentes grupos de medicamentos o combinaciones que pueden alterar directamente la capacidad cognoscitiva como: anticolinérgicos, opioides, benzodiacepinas, hipnóticos, digoxina, antihistamínicos, antidepresivos tricíclicos, relajantes musculares, antiepilépticos y terapia de reemplazo hormonal.
Se hace hincapié en la importancia del examen físico en búsqueda de compromiso neurológico o psiquiátrico, debe buscarse entonces alteraciones del sueńo, alteraciones comportamentales, alucinaciones, parestesias en miembros inferiores, alteraciones en la marcha, entre otras. Lo anterior con el fin de descartar patologías tales como: depresión (para esta patología, recordar el uso de las diferentes escalas como: escala de Hamilton, escala de depresión de estudios epidemiológicos (CES-D), el inventario de depresión de Beck y la Escala de Depresión Geriátrica de Yesavage (Geriatric Depresive Scale: GDS), alteraciones tiroideas, demencias, neuropatías, hipotensión ortostática, accidente cerebrovascular, enfermedad de Parkinson, hidrocefalia de presión normal, entre otras33.
Pruebas Diagnósticas
El DCL es una condición de diagnóstico eminentemente clínico, pero nos podemos ayudar de diferentes pruebas como:
Intervenciones
Se han realizado múltiples estudios, principalmente en el tipo amnésico del DCL, con el fin de postergar o prevenir el progreso a demencia.
Farmacológicamente los inhibidores de la colinesterasa no han demostrado reducir el riesgo de progresión a demencia de uno a tres ańos, además no han mostrado efectos en la función cognoscitiva a corto tiempo (menos de un ańo) y los efectos adversos aumentan exponencialmente37. Varios meta-análisis (uno de 4 estudios con 1960 pacientes, otro de 9 estudios con 5149 pacientes) y en el estudio de Salloway et all38, 2004 con 270 pacientes con DCL, con promedio de edad de 72 ańos y que duró 24 semanas comparando Donepezil 10 miligramos diarios con placebo, no se evidenciaron diferencias estadísticamente significativas. También Petersen et all39, 2005 con 769 pacientes con DCL, comparando Donepezil, Vitamina E 2000 IU/d y placebo durante 3 ańos, sin evidenciar diferencias significativas en la probabilidad de progresión a enfermedad de Alzheimer en el grupo de Vitamina E (HR, 1.02;95% CI, 0.74-1.41; P=0.91) o del Donepezil(HR,0.80;95% CI, 0.57-1.13; P=0.42). Ni el Ginkgo biloba ni la suplementación de testosterona han mostrado mejoría.
Koontz y Baskys40 en el 2005 realizaron un estudio con 19 pacientes con DCL, que duró 4 meses, comparando Galantamina 12 mg dos veces al día contra placebo, midiendo los resultados con el Cambridge Automated Neuropsychiatric Test Assessment Battery (CANTAB), encontrando diferencias entre ambos grupos (SD, 8.3 (1.9) vs 7.0 (1.4; P=0.02)
Hay una reducida evidencia de ensayos clínicos sobre varias intervenciones como el ejercicio aeróbicos o de resistencia vigilados profesionalmente en tienen una pequeńa mejoría en los pacientes con DCL, principalmente en las funciones ejecutivas48; estudios observacionales sugieren que la dieta mediterránea reduce el riesgo de progresión de DCL a demencia50.
Las intervenciones sociales y psicoterapéuticas han mostrado también una mejoría muy limitada.
Un dato fundamental con visión terapéutica y de seguimiento es que los pacientes que revirtieron el DCL presentaban mayor riesgo de volver a presentar DCL y demencia comparados con las personas sin antecedente de DCL41
REFERENCIAS
-
1. Deksnyt? A, Aranauskas R, Budrys V, Kasiulevi?ius V, Sapoka V. delirium: its historical evolution and current interpretation. Eur J Intern Med. 2012;23(6):483-6.
2. Flaherty JH. The evaluation and management of delirium among older persons. Med Clin North Am. 2011;95(3):555-77
3. Inouye SK. delirium in older persons. N Engl J Med 2006;354:1157-65
4. Inouye SK, Westendorp RG, Saczynski JS. delirium in elderly people. Lancet. 2014;383(9920):911-22
5. Egberts A, Fekkes D, Wijnbeld EH, van der Ploeg MA, van Saase JL, Ziere G, van der Cammen TJ, Mattace-Raso FU. Disturbed Serotonergic Neurotransmission and Oxidative Stress in Elderly Patients with delirium. Dement Geriatr Cogn Dis Extra. 2015;5(3):450-8.
6. Kalish VB, Gillham JE, Unwin BK. delirium in older persons: evaluation and management. Am Fam Physician. 2014 Aug 1;90(3):150-8. Review. Erratum in: Am Fam Physician. 2014;90(12):819. Dosage error in article text. Erratum in: Am Fam Physician. 2014;90(12):819
7. Brummel NE, Vasilevskis EE, Han JH, Boehm L, Pun BT, Ely EW. Implementing delirium screening in the ICU: secrets to success. Crit Care Med. 2013;41(9):2196-208.
8. LaMantia MA, Messina FC, Hobgood CD, Miller DK. Screening for delirium in the emergency department: a systematic review. Ann Emerg Med. 2014;63(5):551-560.e2.
9. Zaal IJ, Devlin JW, Peelen LM, Slooter AJ. A systematic review of risk factors for delirium in the ICU. Crit Care Med. 2015;43(1):40-7.
10. Wong CL, Holroyd-Leduc J, Simel DL, Straus SE. Does this patient have delirium?: value of bedside instruments. JAMA. 2010;304(7):779-86.
11. Kalish VB, Gillham JE, Unwin BK. delirium in older persons: evaluation and management. Am Fam Physician. 2014 Aug 1;90(3):150-8. Review. Erratum in: Am Fam Physician. 2014 Dec 15;90(12):819. Dosage error in article text. Erratum in: Am Fam Physician. 2014;90(12):819
12. Budson AE, Price BH. Memory dysfunction. N Engl J Med. 2005; 352:692-699
13. Brandy R. Memory dysfunction. Continuum (Minneap Minn) 2015;21(3):613-626.
14. Scoville WB, Milner B. Loss of recent memory after bilateral hippocampal lesionsJ Neurol Neurosurg Psychiatry 1957;20(1):11-21.
15. Moscovitch M, Cabeza R,Winocur G, Nadel L. Episodic memory and beyond: The hippocampus and neocortex in transformation. Annu Rev Psychol. 2016.67:105-34.
16. Pergola G, Suchan B. Associative learning beyond the medial temporal lobe: many actor son the memory stage. Front Behav Neurosci 2013;7:1-24.
17. Chen KH, Chuan LY, Sim SK, Chee MW. Hippocampal región-specific contributions to memory performance in normal elderly. Brain Cogn 2010;72(3):400-407
18. Pergola G, Gunturkun O, Koch B, et al. Recall deficits in stroke patients with thalamic lesions covary with damage to the parvocellular mediodorsal nucleus of the thalamus. Neuropsychologia 2012;50(10):2477-2491.
19. Bartsch T, Butler C. Transient amnesic syndromes. Nat Rev Neurol 2013;9(2):86-97.
20. Nelson PT, Schmitt FA, Lin Y. Hippocampal sclerosis in advanced age: clinical and pathological features. Brain 2011;134(pt5):1506-1518.
21. Binder J, Desai RH. The neurobiology of semantic memory. Trends Cog Sci 2011;15(11):527-536.
22. Mion M, Patterson K, Acosta-Cabronero J, et al. What the left and right anterior fusiform giry tell us about semantic memory. Brain 2010;133(11):3256-3268.
23. Fletcher PD, Warren JD. Semantic dementia: a specific network-opathy. J Mol Neurosci 2011;45(3):629-636.
24. Rogers TT, Ivanoiu A, Patterson K, Hodges JR. Semantic memory in Alzheimer´s disease and the frontotemporal dementias: a longitudinal study of 236 patients. Neuropsychology 2006;20(3):319-335.
25. BROCKLEHURTS'S. texybook of geriatric medicine and gerontology. 8 edición, 2017. ISBN: 978-0-07020-6185-1.
26. Kandel ER, Dubai Y, Mayford MR. The molecular and systems biology of memory. Cell 2014;157(1):163-186.
27. Foerde K, Shohamy D. The role of the basal ganglia in learning and memory: insight from Parkinson´s disease. Neurobiol Lear Mem 2011;96(4):624-636.
28. Jongsiriyanyong S, Limpawattana P. Mild Cognitive Impairment in Clinical Practice: A Review Article.Am J Alzheimers Dis Other Demen. 2018;33(8):500-507.
29. petersen RC, Lopez O, Armstrong MJ, et al. Practice guideline update summary: mild cognitive impairment: report of the guideline development, dissemination, and implementation subcommittee of the American Academy of Neurology. Neurology.2018;90(3):126-135.
30. Albert MS, DeKosky ST, Dickson D, et al. The diagnosis of mild cognitive impairment due to Alzheimer´s desease: recommendations from the National Institute on Aging-Alzheimer´s Association Workgroups on Diagnostic guidelines for Alzheimer´s disease. Alzheimers Dement.2011;7(3):270-279
31. Buratti L, Balestrini S, Altamura C, Viticchi G, Falsetti, Luzzi S, Provinciali L, Vernieri F, Silvesrini M. Markers of the risk of progression from mild cognitive impairment to Alzheimer´s disease. J Alzheimers Dis. 45(3)(2015)883-890.
32. Langa KM, Levine DA. The diagnosis and management of mild cognitive impairment. A clinical review. JAMA.2014;312(23):2551-2561.
33. Petersen RC. Clinical practice: mild cognitive impairment. N Engl J Med. 2011; 364(23): 2227-2234
34. Gagnon G, Hansen KT, Woolmore-Goodwin S, et al. Correcting the MoCA for education: effect on sensitivity. Can J Neurol Sci. 2013;40(5):678-683.
35. Espino DV, Lichtenstein MJ, Palmer RF, Hazuda HP. Ethnic differences in Mini-Mental State Examination (MMSE) scores: where you live makes a difference. J Am Geriatr Soc. 2001;49(5):538-548.
36. Jack CR. Barkhof F, Bernstein MA, et al. Steps to standarization and validation of hipocampal volumetry as a biomarker in clinical trials and Diagnostic criterion for Alzheimer´s disease. Alzheimers Dement.2011;7(4):474-485.
37. Russ TC, Morling JR. Cholinesterase inhibitors for mild cognitive impairment. Cochrane Database Syst Rev. 2012;9:CDOO9132.
38. Doody RS, Ferris SH, Salloway S, et al. Donepezil treatment of patients with MCI: a 48 week randomized, placebo-controlled trial. Neurology. 2009;72(18):1555-1561.
39. Petersen RC, Thomas RG, Grundman M, et al. Vitamin E and donepezil for the treatment of mild cognitive impairment. N Engl J Med. 2005;352(23): 2379-2388
40. Koontz J, Baskys A. Effects of galantamine on Working memory and global functioning in patients with mild cognitive impairment. Am J Alzheimers Dis Other Demen. 2005;20(5):295-302.
41. Koepsell TD, Monsell SE. Reversion from mild cognitive impairment to normal o near-normal cognition. Neurology.2012;79(15):1591-1598.
Comentario de la revisora Dra. Cynthia Marińansky . Geriatra de planta de la Unidad de Geriatria del Hospital Durand de Buenos Aires Directora de la Especialización en Geriatria Universidad Maimonides..
La comprensión y diagnóstico del síndrome confusional agudo a la luz de su fisiopatología y consecuencias, es crucial en Medicina Geriátrica. El trabajo brinda herramientas para lograr este objetivo.
Comentario de la revisora Dra Silvina Dahl. Geriatra. Hogar Ledor Vador, Buenos Aires. Argentina
En el marco de una población que envejece, dentro de las patologías prevalentes en las personas mayores se encuentran lo que podríamos denominar las 3D: Demencia, delirium y Depresión. El trabajo que nos presentan los autores constituye un estudio pormenorizado de las dos primeras; así como del entrecruzamiento de ambos cuadros.
